|
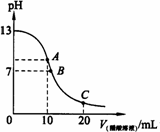
25℃时,在20ml0.1mol·L-1NaOH溶液中逐滴加入0.2mol·L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是
| |
| [ ] | |
A. |
在A点: |
B. |
在B点: |
C. |
在C点: |
D. |
在C点: |
|
从海水中提镁,最基本的方法是往海水里加碱,得到Mg(OH)2沉淀,将沉淀分离出来后再加入盐酸把它变成MgCl2;之后,经过滤、干燥、电解,即可得到金属镁.下列对从海水中提镁的有关说法中,正确的是 | |
| [ ] | |
A. |
整个过程中没有涉及置换反应 |
B. |
往海水里加碱是指直接加入Ca(OH)2 |
C. |
电解MgCl2溶液即可得到金属镁 |
D. |
电解时得到的镁蒸气应在CO2氛围中冷却 |
|
右图是硫酸试剂瓶标签上的部分内容.据此下列说法中,正确的是
| |
| [ ] | |
A. |
该硫酸可以用来干燥硫化氢气体 |
B. |
1molZn与足量的该硫酸反应能产生2gH2 |
C. |
配制200ml4.6mol·L-1的稀硫酸需取该硫酸50ml |
D. |
若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗 |
|
设NA表示阿伏加德罗常数,下列叙述中,正确的是 | |
| [ ] | |
A. |
常温常压下,16gO2和O3的混合物中共含有NA个氧原子 |
B. |
假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA |
C. |
78gNa2O2固体中所含阴、阳离子总数为4NA |
D. |
在铜与硫的反应中,1mol铜原子参加反应失去的电子数为2NA |
|
下列叙述中,正确的是 | |
| [ ] | |
A. |
胶体微粒能透过半透膜和滤纸 |
B. |
SO2能使溴水退色,这一事实说明SO2具有漂白性 |
C. |
铁制品在空气中生锈主要发生的是析氢腐蚀 |
D. |
金刚石、石墨与C60都是碳元素的同素异形体 |
|
核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为(2n+1),原子核内质子数为(2n2-1).下列关于元素X的说法中,不正确的是 | |
| [ ] | |
A. |
其最高化合价为+3价 |
B. |
可以形成化学式为KXO3的盐 |
C. |
其氢化物可以用来做喷泉实验 |
D. |
其最高价氧化物的水化物是强酸 |
|
14 C是一种放射性同位素,在高层大气中由宇宙射线产生的中子或核爆炸产生的中子轰击14N可使它转变为14C,14N+ | |
| [ ] | |
A. |
14 C和14N互为同位素 |
B. |
14 C和C60是同素异形体 |
C. |
14 CO2的摩尔质量为46 |
D. |
地球上活着的生物体内,由于新陈代射作用也存在14C |
|
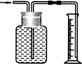
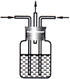
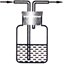
张老师做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成有少量KSCN和FeCl2溶液,溶液显红色.判断下列说法中正确的是
| |
| [ ] | |
A. |
该条件下生成的水分子化学性质比较活泼 |
B. |
该条件下H2被冷却为液态氢,液氢的水溶液具有还原性 |
C. |
该条件下H2燃烧生成了只具有氧化性的物质 |
D. |
该条件下H2燃烧的产物中可能含有一定量的H2O2 |
|
有一无色溶液,可能含有K+、Al3+、Mg2+、 | |
| [ ] | |
A. |
肯定有K+、 |
B. |
肯定有Al3+、Mg2+、 |
C. |
肯定有Al3+、Mg2+、 |
D. |
肯定有Al3+、Mg2+、 |