|
在硫酸铝、硫酸钾和明矾的混合溶液中,如果[SO42-]=0.2mol昄-1,当加等体积的0.2mol昄-1的KOH溶液时,生成沉淀恰好溶解,则原混合物中K+的浓度是 | |
| [ ] | |
A. |
0.2mol昄-1 |
B. |
O.25mol昄-1 |
C. |
O.45mol昄-1 |
D. |
O.225mol昄-1 |
|
19.2毫克铜跟适量的浓硝酸反应,铜全部作用后共收集到气体8.96毫升(标准状况),反应消耗的HNO3的物质的量可能是( )×10-3摩尔.(不考虑NO2与N2O4之间的转化) | |
| [ ] | |
A. |
0.8 |
B. |
0.9 |
C. |
1.0 |
D. |
1.2 |
|
镁铁混合物4.9g,溶解在过量某浓度的稀硝酸中,完全反应得到标况下气体2.24L(假设气体全为NO),则向反应后的溶液中加入足量的烧碱,则可生成沉淀的量是 | |
| [ ] | |
A. |
6g |
B. |
8g |
C. |
10g |
D. |
12g |
|
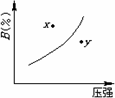
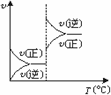
mA(固)+nB(气)
| |
| [ ] | |
A. |
m+n<p |
B. |
x点的状态是v正>v逆 |
C. |
n>p |
D. |
x点比y点的反应速度慢 |
|
已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是 | |
| [ ] | |
A. |
2C2H2(g)+5O2(g) |
B. |
C2H2(g)+5/2O2(g) |
C. |
2C2H2(g)+5O2(g) |
D. |
2C2H2(g)+5O2(g) |
|
在100mL某混合溶液中,C(HNO3)=0.4mol/L,C(H2SO4)=0.1mol/L.向其中加入1.92g铜粉,微热,充分反应后溶液中C(Cu2+)为(假设溶液体积不变) | |
| [ ] | |
A. |
0.15mol/L |
B. |
0.3mol/L |
C. |
0.225mol/L |
D. |
无法计算 |
|
同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2.现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是 | |
| [ ] | |
A. |
V1>V2>V3 |
B. |
V1>V3>V2 |
C. |
V2>V3>V1 |
D. |
V3>V1>V2 |
|
用NA表示阿伏加德罗常数的值,下列说法中正确的是 | |
| [ ] | |
A. |
6.2克白磷分子中含P—P键为0.05NA |
B. |
将含有NO2和N2O4分子共约NA个的混合气,温度降至标准状况,其体积约为22.4L |
C. |
6.4gS6与S8的混合物中所含S原子数一定为0.2NA |
D. |
标准状况下,2.24L氧单质所含原子数一定为0.2NA |
|
50g浓度为cmol/L、密度为ρg/cm3的氨水中加入一定量的水稀释成0.5cmol/L,则加入水的体积为 | |
| [ ] | |
A. |
小于50mL |
B. |
等于50mL |
C. |
大于50mL |
D. |
等于50/ρmL |