|
下列有关阿伏加德罗常数的叙述正确的是: | |
| [ ] | |
A. |
0.1mol碳酸钠溶于水所得溶液中所含阴离子数小于0.1×6.02×1023个 |
B. |
标准状况下,0.5×6.02×1023个甲醛分子所占体积约是11.2L |
C. |
1mol冰醋酸中含有6.02×1023个CH3COO?/P> |
D. |
标准状况下,含4molHCl的浓盐酸与足量MnO2反应可生成22.4LCl2 |
|
下列可用氢键来解释的是: | |
| [ ] | |
A. |
浓的氢氟酸溶液中存在HF2-和H2F3- |
B. |
SiH4沸点比CH4高 |
C. |
水和乙醇分别与金属钠反应,前者比后者剧烈 |
D. |
H2O比H2S稳定,前者1000oC以上才分解,后者300oC分解 |
|
下列事实不能用勒夏特列原理解释的是: | |
| [ ] | |
A. |
氨水应密闭保存,放置于低温处 |
B. |
在硫酸亚铁溶液中,加入铁粉以防止氧化变质 |
C. |
生产硝酸的过程中使用过量空气以提高氨气的利用率 |
D. |
实验室常用排饱和食盐水的方法收集氯气 |
|
六氟化硫分子呈正八面体,难以水解,在高电压下仍有良好的绝缘性,在电器行业有着广泛用途,但逸散到空气中会引起强温室效应.下列有关SF6的推测正确的是: | |
| [ ] | |
A. |
SF6易燃烧生成二氧化硫 |
B. |
SF6中各原子均达到八电子稳定结构 |
C. |
高温条件下,SF6微弱水解生成H2SO4和HF |
D. |
SF6是极性分子 |
|
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB=2VC,且VA=VB+VC,则在C的生成物中,该金属元素的化合价为 | |
| [ ] | |
A. |
+1 |
B. |
+2 |
C. |
+3 |
D. |
+4 |
|
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol/L,则此溶液最多可溶解铁粉的质量为 | |
| [ ] | |
A. |
11.2克 |
B. |
16.8克 |
C. |
19.6克 |
D. |
22.4克 |
|
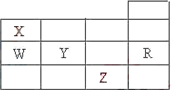
右表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| |
| [ ] | |
A. |
常压下五种元素的单质中,Z单质的沸点最高 |
B. |
Y、Z的阴离子电子层结构都与R原子的相同 |
C. |
W的氢化物的沸点比X的氢化物的沸点高 |
D. |
Y元素的非金属性比W元素的非金属性强 |