|
常温下,下列各组离子在指定环境下能大量共存的是 | |
| [ ] | |
A. |
pH=l的溶液中:Na+、K+、SO32-、MnO4- |
B. |
pH=7的溶液中:Na+、A13+、Cl-、SO42- |
C. |
pH>12的溶液中:Na+、K+、SO42-、AlO2- |
D. |
pH=0的溶液中:Na+、K+、NO3-、ClO- |
|
常温下单质硫主要以S8形式存在.加热时,S8会转化为S6、S4、S2等.当温度达到750℃时,硫蒸汽主要以S2形式存在(占92%).下列说法正确的是 | |
| [ ] | |
A. |
S8转化为S6、S4、S2属于物理变化 |
B. |
不论哪种硫分子,完全燃烧都生成SO2 |
C. |
常温条件下单质硫为原子晶体 |
D. |
把硫单质在空气种加热到750℃即得S2 |
|
在密闭容器中,对已达到化学平衡的反应:2A(g)+B(g) ①升高温度时c(B)/c(C)的比值变小 ②降低温度时,体系内混合气体的平均式量变小 ③加入B后,A的转化率增大 ④加入催化剂,气体总的物质的量不变 ⑤加入C后,则A、B的物质的量均增大 | |
| [ ] | |
A. |
②③⑤ |
B. |
③④⑤ |
C. |
①②③⑤ |
D. |
全部 |
|
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是
| |
| [ ] | |
A. |
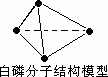
31g白磷分子(P4)中含有P—P键个数为1.5×6.02×1023 |
B. |
48gO2和48gO3所含分子数为3×6.02×1023 |
C. |
1.0L1mol/L氨水中,NH3·H2O的分子数为6.02×1023 |
D. |
20g重水(D2O)中含有的中子数为8×6.02×1023 |
|
密闭容器中,300℃时将100mL由H2O、CO2、H2和CO组成的混合气体与足量的Na2O2在连续电火花作用下充分反应后,容器内压强只有原来的五分之一,则原混合气体中各组分的体积比不可能是 | |
| [ ] | |
A. |
1∶1∶1∶1 |
B. |
3∶1∶2∶4 |
C. |
1∶3∶5∶1 |
D. |
2∶2∶3∶3 |
|
已知A2On2-可与B2-反应,B2-被氧化为B单质,A2On2-被还原为A3+,若100mL0.3mol·L-1的A2On2-溶液,与150mL0.6mol·L-1的B2-溶液恰好完全反应,则n的值为 | |
| [ ] | |
A. |
5 |
B. |
6 |
C. |
7 |
D. |
8 |
|
下列热化学方程式中△H的数值能表示可燃物燃烧热的是 | |
| [ ] | |
A. |
CO(g)+ |
B. |
CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-802.3kJ/mol |
C. |
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol |
D. |
H2(g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol |
|
T℃时,A气体与B气体反应生成C气体.反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
| |
| [ ] | |
A. |
在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
B. |
(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
C. |
T℃时,在相同容器中,若由0.3mol·L—1A、0.1mol·L—1B和0.4mol·L—1C混合反应,达到平衡后,C的浓度仍为0.4mol·L—1 |
D. |
其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |