|
某无色溶液中滴入酚酞试液显红色,该溶液中可以大量共存的离子组是 | |
| [ ] | |
A. |
Mg2+、Al3+、HCO3-、SO32- |
B. |
K+、Na+、AlO2-、NO3- |
C. |
K+、Ca2+、MnO4-、Cl- |
D. |
NH4+、Fe3+、SO42-、SCN- |
|
下列有关化学实验的操作或说法中,正确的是 | |
| [ ] | |
A. |
配制氯化铁溶液时,先将氯化铁溶于浓盐酸,再用蒸馏水稀释并加入适量铁粉 |
B. |
用加热法测定硫酸铜晶体中结晶水含量时,若在空气中冷却会使结果偏低 |
C. |
将浓硫酸在量筒中稀释 |
D. |
将锌粒投入CuSO4溶液中充分反应后,固体质量一定增加 |
|
发生原电池的反应通常是放热反应,在理论上可设计成原电池的化学反应是 | |
| [ ] | |
A. |
C(s)+H2O(g)=CO(g)+H2(g);△H>0 |
B. |
Ba(OH)2·8H2O+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(l)+8H2O(l);△H>0 |
C. |
CaC2(s)+2H2O(l)=Ca(OH)2(s)+C2H2(g);△H<0 |
D. |
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H<0 |
|
设NA为阿伏加德罗常数,下列叙述正确的是 | |
| [ ] | |
A. |
1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒 |
B. |
标准状况下,2.24L乙醛完全燃烧所得CO2分子数为0.2NA |
C. |
1L0.1mol·L-1的醋酸溶液中的分子总数大于0.1NA |
D. |
通过化学反应制得1molO2,转移电子的数目一定是4NA |
|
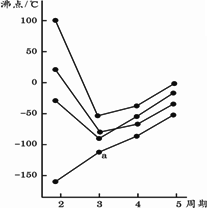
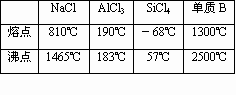
根据表中给出的几种物质在常压下的熔、沸点数据,判断下列有关说法中错误的是
| |
| [ ] | |
A. |
SiCl4形成的晶体是分子晶体 |
B. |
单质B可能是原子晶体 |
C. |
电解NaCl水溶液可制得金属钠 |
D. |
不能用电解熔融AlCl3制取单质铝 |
|
已知几种阴离子还原性强弱顺序为OH-<Cl-<Br-<I-<S2-.若在某溶液含有相同浓度的OH-、Cl-、Br-、I-、S2-,当向其中逐滴加入新制的饱和氯水直至过量时,最后被氧化的离子是 | |
| [ ] | |
A. |
Br- |
B. |
Cl- |
C. |
OH- |
D. |
S2- |
|
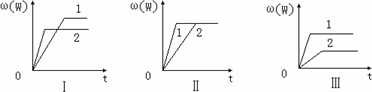
在一密闭容器中有如下反应:aX(g)+bY(g)
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.当其它条件不变时,下列分析正确的是 | |
| [ ] | |
A. |
图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b>n |
B. |
图II可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好 |
C. |
图III可能是不同压强对反应的影响,且P1>P2,n>a+b |
D. |
图III可能是不同温度对反应的影响,且T1>T2,ΔH<0 |
|
下列叙述正确的是 | |
| [ ] | |
A. |
0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若有c(CH3COO-)>c(Na+),则混合液一定呈碱性 |
B. |
常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7, |
C. |
0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=c(H2A)+c(HA-)+2c(A2-) |
D. |
将5mL0.02mol/L的H2SO4与5mL0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2 |