|
通常状况下,前者一定大于后者的是 | |
| [ ] | |
A. |
物质的量浓度相等的次氯酸钠溶液和醋酸钠溶液的pH |
B. |
25℃的纯水和100℃的纯水中的c(H+) |
C. |
硫酸铵溶液和氯化铵溶液中c(NH4+) |
D. |
读取量筒中一定体积的液体时,仰视的读数和俯视的读数 |
|
100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ①烧瓶内气体的颜色不再加深,②N2O4的消耗速率与NO2的生成速率之比为1∶2,③NO2的生成速率与NO2消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体平均相对分子质量不再变化 | |
| [ ] | |
A. |
②⑤⑦ |
B. |
①③④⑥⑧ |
C. |
只有③ |
D. |
只有⑤ |
|
2005年10月12日我国成功发射了第二艘载人航天飞船——“神州六号”,实现了双人多天太空旅行.这标志着中国人的太空时代又前进了一大步.发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气. 已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ/mol N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=–534kJ/mol 下列关于肼和NO2反应的热化学方程式中,正确的是 | |
| [ ] | |
A. |
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=–1135.7kJ/mol |
B. |
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=–1000.3kJ/mol |
C. |
N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=–1135.7kJ/mol |
D. |
2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=–1135.7kJ/mol |
|
已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化: H2O2→H2OIO3→I2MnO4→Mn2+HNO3→NO 如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是 | |
| [ ] | |
A. |
H2O2 |
B. |
IO3?/P> |
C. |
MnO4?/P> |
D. |
HNO3 |
|
下列有关物质的结构或性质的叙述错误的是 | |
| [ ] | |
A. |
由极性键形成的分子不一定是极性分子 |
B. |
水是一种非常稳定的化合物,这是由于氢键所致 |
C. |
石英、食盐、金属钠、干冰的熔点依次降低 |
D. |
分子晶体中一定存在分子间作用力,可能有共价键 |
|
下列各组有机物,不论以何种比例混合,只要二者物质的量之和不变,那么,完全燃烧时所消耗氧气的物质的量相等,且所生成的物质的量也相等的是 | |
| [ ] | |
A. |
甲烷和甲酸甲酯 |
B. |
乙烷和乙醇 |
C. |
苯和苯酚 |
D. |
乙炔和苯 |
|
下列热化学式中△H的绝对值能表示可燃物燃烧热的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
过氧化氢俗称双氧水,它是一种液体,易分解,常作氧化剂、漂白剂,为贮存、运输、使用的方便,YC工业上常将H2O2转化为固体的过碳酸钠(化学式为:2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质.下列物质不会使过碳酸钠晶体失效的是 | |
| [ ] | |
A. |
MnO2 |
B. |
H2S |
C. |
NaHCO3 |
D. |
稀HCl |
|
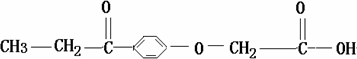
利尿酸在奥运会上被禁用,其结构简式为:
下列叙述正确的是 | |
| [ ] | |
A. |
利尿酸分子内处于同一平面的原子数不超过10个 |
B. |
利尿酸能使溴水褪色 |
C. |
1mol利尿酸最多可与6molH2发生加成反应 |
D. |
利尿酸与新制Cu(OH)2悬浊液反应有红色沉淀生成 |