|
下列离子方程式正确的是 | |
| [ ] | |
A. |
澄清石灰水中滴加稀硝酸: Ca(OH)2+2H+ |
B. |
用Pt电极电解饱和氯化镁溶液: 2Cl-+2H2O |
C. |
向FeBr2溶液中通入过量氯气: 2Fe2++Cl2 |
D. |
向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液: Ca2++2HCO3-+2OH- |
|
将两个铂电极插入500毫升CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化).此时溶液中氢离子浓度约为 | |
| [ ] | |
A. |
4×10-3mol/L |
B. |
2×10-3mol/L |
C. |
3×10-3mol/L |
D. |
1×10-3mol/L |
|
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的几种.现取该溶液进行实验,得到如下现象: ①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出; ②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成; ③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色. 据此可以推断:该溶液中肯定不存在的离子是 | |
| [ ] | |
A. |
Al3+、Mg2+、I-、SO32- |
B. |
Mg2+、Na+、CO32-、I- |
C. |
Al3+、Na+、SO32-、I- |
D. |
Al3+、CO32-、Br-、SO32- |
|
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍(已知:氧化性Fe2+<Ni2+<Cu2+),下列叙述正确的是 | |
| [ ] | |
A. |
阳极发生还原反应,其电极反应式:Ni2++2e-==Ni |
B. |
电解过程中,阳极质量的减少与阴极质量的增加相等 |
C. |
电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
D. |
电解后,电解槽底部的阳极泥中只有Cu和Pt |
|
在盛有饱和Na2CO3溶液的烧杯中,插入惰性电极,保持温度不变,通电一定的时间后,下列判断正确的是 | |
| [ ] | |
A. |
溶液的pH将增大 |
B. |
Na+数和CO32-数的比值将变小 |
C. |
溶液浓度不变,有晶体析出 |
D. |
溶液浓度逐渐增大并有晶体析出 |
|
常温下,下列各组物质不能用一种试剂通过化学反应区别的是 | |
| [ ] | |
A. |
MnO2 CuO FeO |
B. |
Na2CO3 NaHCO3 K2CO3 |
C. |
AgNO3 KNO3 Na2CO3 |
D. |
(NH4)2SO4 K2SO4 NH4Cl |
|
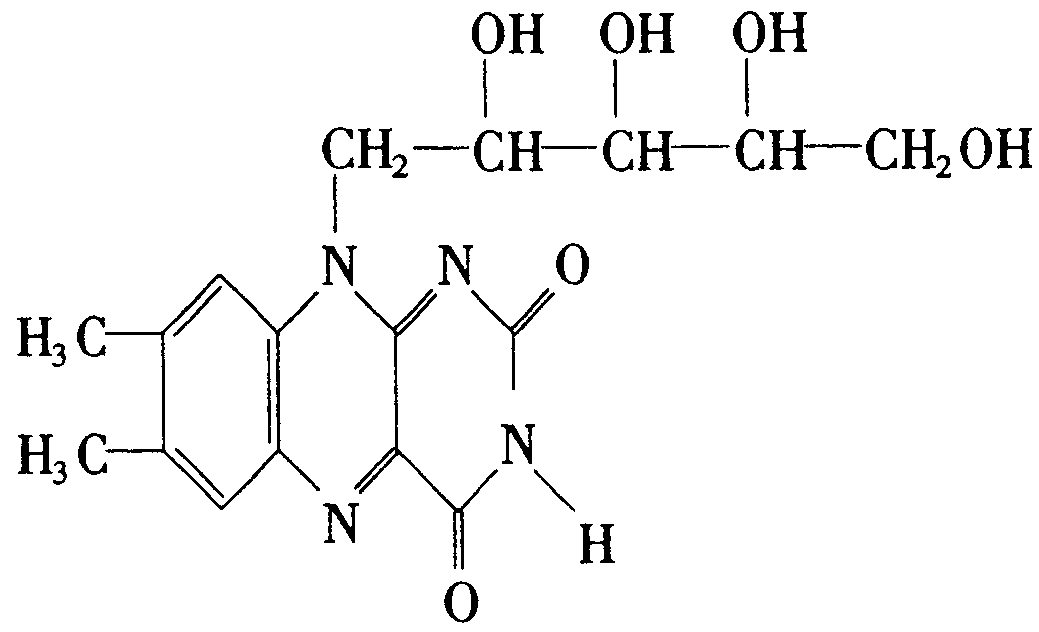
维生素B2也称“核黄素”,其结构如下图.维生素B2的磷酸盐衍生物是某些氧化还原酶的辅基,为生长必需物质,缺少维生素B2会引起口角炎、皮肤和眼部疾病.下列有关维生素B2的说法中正确的是
| |
| [ ] | |
A. |
核黄素晶体属于离子晶体 |
B. |
核黄素能发生银镜反应 |
C. |
核黄素能被酸性高锰酸钾溶液氧化 |
D. |
核黄素能与氯化铁溶液作用呈紫色 |
|
对于某酸性溶液(可能含有Br–、SO42–、H2SO3、NH4+),分别进行如下实验:①加热时放出的气体可使品红溶液褪色 ②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝 ③加入氯水时,溶液略呈橙红色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀.对于下列物质不能确定其在原溶液中是否存在的是 | |
| [ ] | |
A. |
Br– |
B. |
SO42– |
C. |
H2SO3 |
D. |
NH4+ |
|
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组是 | |
| [ ] | |
A. |
Ba(OH)2 KSCN NaCl Mg(NO3)2 (FeCl3溶液) |
B. |
NaNO3 NaHCO3 (NH4)2SO3 Na2SiO3 (H2SO4溶液) |
C. |
NH4Br K2CO3 NaI CaCl2 (AgNO3溶液) |
D. |
(NH4)3PO4 NaBr CuSO4 AlCl3 (KOH溶液) |
|
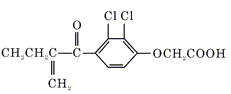
利尿酸在奥运会上被禁用,其结构简式如图所示.下列叙述正确的是
| |
| [ ] | |
A. |
利尿酸衍生物利尿酸甲脂的分子式是C14H14Cl2O4 |
B. |
利尿酸分子内处于同一平面的原子不超过10个 |
C. |
1 mol利尿酸能与7 mol H2发生加成反应 |
D. |
利尿酸能与FeCl3溶液发生显色反应 |