|
下列叙述中指定粒子的数目大于6.02×1023的是 | |
| [ ] | |
A. |
2g重水(D2O,D为 |
B. |
0.1molF—中含有的电子数 |
C. |
标准状况下,11.2LN2和NO混合气体中的原子数 |
D. |
1L1mol·L—1Na2SO4溶液中的Na+离子数 |
|
(1)指出下列实验用品或仪器(已洗涤干净)使用时的第一步操作: ①石蕊试纸(检验气体性质)________ ②容量瓶________ (2)右图分别是温度计、量筒、滴定管的一部分,下述读数及说法正确的是________.
| |
| [ ] | |
A. |
①是量筒,读数为2.5mL |
B. |
②是量筒,读数为2.5Ml |
C. |
③是滴定管,读数为3.5mL |
D. |
①是温度计,读数为2.5℃ |
|
某二元酸(H2A)按下式发生电离:H2A=H++HA-;HA- ①0.01mol/L的H2A溶液②0.01mol/L的NaHA溶液 ③0.02mol/L的HCl溶液与0.04mol/L的NaHA溶液等体积混合 ④0.02mol/L的NaOH溶液与0.02mol/L的NaHA溶液等体积混合 | |
| [ ] | |
A. |
四种溶液中c(HA-)浓度大小:③>①>②>④ |
B. |
溶液①中粒子浓度大小顺序是:c(H2A)>c(H+)>c(HA-)>c(A2-)>c(OH-) |
C. |
溶液②中有关离子浓度关系:c(HA-)+2c(A2-)+c(H2A)=c(Na+) |
D. |
溶液③中有关离子浓度关系:c(HA-)+c(A2-)+c(OH-)=c(Na+)+c(H+) |
|
室温下,由水电离得到的c(H+)为1×10-12的无色溶液中,可能大量共存的离子组有: | |
| [ ] | |
A. |
K+、S2-、HSO3-、Na+ |
B. |
I-、Na+、SO42-、NO3- |
C. |
Na+、Fe2+、Br-、Cl- |
D. |
AlO2-、K+、NH4+、Na+ |
|
如图是在MgCl2、AlCl3混和溶液中,加入a或b时,沉淀物的量与加入的a或b的量的关系图,以下结论正确的是
①T之前加NaOH溶液,T之后加盐酸 ②T之前加盐酸,T之后加NaOH溶液 ③混和液c(AlCl3)∶c(MgCl2)=1∶1 ④图中所消耗的NaOH和HCl物质的量之比是3∶1 ⑤该盐酸与NaOH溶液的物质的量浓度相同 | |
| [ ] | |
A. |
①③④ |
B. |
①③⑤ |
C. |
②③④ |
D. |
②③⑤ |
|
将2molX、3molZ两种气体混合于某体积不变的密闭容器内发生如下反应: 2X(g)+Y(g) | |
| [ ] | |
A. |
3.2molX、0.6molY、1.2molZ |
B. |
3.6molX、1molY、0.6molZ |
C. |
2.8molX、0.4molY、1molZ |
D. |
2.2molX、0.2molY、2.4molZ |
|
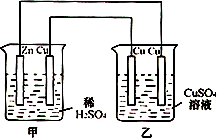
下列关于右图装置的说法中,错误的是
| |
| [ ] | |
A. |
甲池是原电池,乙池是电解池 |
B. |
甲池的PH将增大 |
C. |
乙池中c(Cu2+)保持不变 |
D. |
甲池中Zn溶解的物质的量小于乙池中阳极Cu 溶解的物质的量 |
|
恒温、恒压下,1molA和nmolB在一个容积可变的容器中发生如下反应:A(g)+2B(g) | |
| [ ] | |
A. |
若起始时放入3molA和3nmolB,则达平衡时生成3amolC |
B. |
起始时刻和达平衡后容器中的压强比为(1+n):(1+n— |
|
拟晶(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质.Al65Cu23Fe12是2000年之前发现的几百种拟晶之一,具有合金的某些优良物理性能.有关这种拟晶的说法错误的是 | |
| [ ] | |
A. |
Al65Cu23Fe12的硬度比金属Al、Cu、Fe都大 |
B. |
Al65Cu23Fe12中三种金属的化合价均可视作零 |
C. |
Al65Cu23Fe12不可用作长期浸泡在海水中的材料 |
D. |
1molAl65Cu23Fe12溶于过量的硝酸时共失去265mol电子 |
|
甲、乙两种物质的溶解度曲线如右图所示:下列说法一定正确的是
| |
| [ ] | |
A. |
A点表示T1℃时甲的溶液已饱和,乙的溶液未饱和 |
B. |
B点表示T2℃时甲、乙两物质的溶液均达饱和且两 溶液的物质的量浓度相等 |
C. |
将T3℃时甲、乙两物质的饱和溶液分别降温至T2℃, 析出的乙比析出的甲多 |
D. |
若乙中含有少量的甲,可用重结晶的方法提纯乙 |