|
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH.则电解过程中转移的电子数为 | |
| [ ] | |
A. |
0.1mol |
B. |
0.2mol |
C. |
0.3mol |
D. |
0.4mol |
|
有物质的量浓度、体积都相同的NaF溶液和NaCN溶液.已知HF比HCN较易电离.则溶液中离子总数的关系正确的是 | |
| [ ] | |
A. |
NaF=NaCN |
B. |
NaF>NaCN |
C. |
NaF<NaCN |
D. |
无法确定 |
|
温度为25℃时,将两个铂电极插入一定量的硫酸钠饱和溶液中进行电解,通电一段时间后,在阳极逸出amol气体,同时有WgNa2SO4·10H2O析出,若温度不变,此时剩余溶液中溶质的质量分数为 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
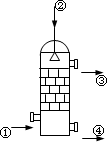
在硫酸工业生产中,SO3的吸收过程是在吸收塔(如右图)中进行的,吸 收塔里还装入了大量瓷环.下列有关SO3说法中,不正确的是:
| |
| [ ] | |
A. |
从①处通入SO3,整个吸收操作采取逆流的形式 |
B. |
从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积 |
C. |
从③处导出的气体只含有少量SO2,可直接排入大气 |
D. |
从④处流出的是可用水或稀硫酸稀释的硫酸 |
|
已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为 C(石墨)+O2(g)===CO2(g)△H=-393.51kJ·mol-1 C(金刚石)+O2(g)===CO2(g)△H=-395.41kJ·mol-1,据此判断,下列说法正确的是 | |
| [ ] | |
A. |
由石墨制备金刚石中吸热反应;等质量时,石墨的能量比金刚石的低 |
B. |
由石墨制备金刚石中吸热反应;等质量时,石墨的能量比金刚石的高 |
C. |
由石墨制备金刚石中放热反应;等质量时,石墨的能量比金刚石的低 |
D. |
由石墨制备金刚石中放热反应;等质量时,石墨的能量比金刚石的高 |
|
国外最新研制的溴——锌蓄电池的基本结构是用碳棒作两极,电解质是溴化锌溶液.现有四个电极反应:①Zn-2e-=Zn2+②Zn2++2e-=Zn③Br2+2e-=2Br-④2Br--2e-=Br2.那么充电时的阳极反应和放电时的负极反应分别是 | |
| [ ] | |
A. |
④① |
B. |
②③ |
C. |
③① |
D. |
②④ |
|
近年来,加“碘”食盐较多的使用了碘酸钾(KIO3),碘酸钾在工业上可用电解法制取.以石墨和不锈钢为电极,以KI溶液为电解液,在一定条件下电解,反应方程式为: KI+3H2O | |
| [ ] | |
A. |
电解时,石墨作阴极,不锈钢作阳极 |
B. |
电解时,阳极反应是:I––6e–+3H2O=IO3–+6H+ |
C. |
溶液调节至强酸性,对生产有利 |
D. |
电解前后溶液的pH升高 |
|
下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是 | |
| [ ] | |
A. |
H2(g)+Cl2(g)=2HCl(g);△H=-184.6kJ/mol |
B. |
CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H=-802.3kJ/mol |
C. |
2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol |
D. |
CO(g)+1/2O2(g)=CO2(g);△H=-283kJ/mol |