|
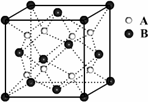
阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是 | |
| [ ] | |
A. |
标准状况下,1.12L的SO3所含的原子数约为0.2×6.02×1023 |
B. |
在标准状况下,2.24L一氧化氮与氮气混合气所含分子数约为0.1×6.02×1023 |
C. |
1molCH3+(碳正离子)中含电子数目约为10×6.02×1023 |
D. |
1molD2O含有的中子数约为8×6.02×1023 |
|
将0.1L含有0.02molCuSO4和0.01molNaCl的水溶液用惰性电极电解.电解一段时间后,一个电极上得到0.01molCu,另一电极析出的气体 | |
| [ ] | |
A. |
只有Cl2 |
B. |
只有O2 |
C. |
既有Cl2又有O2 |
D. |
只有H2 |
|
对下列各种溶液中所含离子的判断合理的是 | |
| [ ] | |
A. |
向无色溶液中加氯水变橙色,溶液中可能含:SO42棧—Br棧—OH棧—Ba2+ |
B. |
在c(H+)=10-14mol/L的溶液中可能含:Na+,A102棧—CO32棧—SO32?/P> |
C. |
某溶液,加铝粉有氢气放出,则溶液中可能含:K+,Na+,H+,NO3- |
D. |
使紫色石蕊试液变红色的溶液中可能含:K+,Na+,Ca2+,HC03?/P> |
|
肼(N2H4)是火箭发动机的燃料,反应时N2O4为氧化剂,生成氮气和水蒸气.已知: N2(g)+2O2(g)=N2O4(g);△H=+8.7kJ/mol N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534.0kJ/mol 下列表示肼跟N2O4反应的热化学方程式,正确的是 | |
| [ ] | |
A. |
2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-542.7kJ/mol |
B. |
2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1059.3kJ/mol |
C. |
2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g);△H=-1076.7kJ/mol |
D. |
N2H4(g)+ |
|
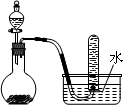
右图是制取和收集某气体的实验装置,该装置可用于
| |
| [ ] | |
A. |
用浓盐酸和二氧化锰反应制取Cl2 |
B. |
用浓氨水和生石灰反应制取NH3 |
C. |
用浓硝酸与铜反应制取NO2 |
D. |
用过氧化钠固体和水反应制取O2 |
|
向一定量的Fe、Fe3O4的混合物中,加入200mL1mol/L的盐酸,恰好使混合物完全溶解,放出448mL(S、T、P)的气体.所得溶液中加入KSCN溶液无血红色出现,混合物中铁元素的质量分数为 | |
| [ ] | |
A. |
68.6% |
B. |
77.8% |
C. |
81.4% |
D. |
无法计算 |
|
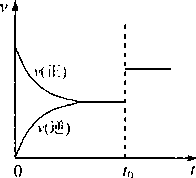
可逆反应aX(g)+bY(g)
| |
| [ ] | |
A. |
若a+b=c,则t0时只能是增大了容器的压强 |
B. |
若a+b=c,则t0时只能是加入了催化剂 |
C. |
若a+b≠c,则t0时只能是加入了催化剂 |
D. |
若a+b≠c,则t0时只能是增大了容器的压强 |
|
恒温下,将两个铂电极插入一定量的Na2SO4饱和溶液里进行电解,经过一段时间后,在阳极逸出nmol气体,同时从溶液中析出mgNa2SO4·10H2O晶体,则原Na2SO4溶液的质量分数为 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|