|
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) | |
| [ ] | |
A. |
阳极发生还原反应,其电极反应式:Ni2++2e- |
B. |
电解过程中,阳极质量的减少与阴极质量的增加相等 |
C. |
电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
D. |
电解后,电解槽底部的阳极泥中只有Cu和Pt |
|
已知0.1mol/L的二元酸H2A溶液的pH=4.0,则下列说法中正确的是 | |
| [ ] | |
A. |
在Na2A、NaHA两溶液中,离子种类不相同 |
B. |
在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等 |
C. |
在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-) |
D. |
在Na2A溶液中一定有:c(Na+)>c(A2-)>c(H+)>c(OH-) |
|
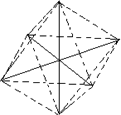
已知[Co(NH3)6]3+呈正八面体结构,若其中有两个NH3分子分别被H2O取代,所形成的[Co(NH3)4(H2O)2]3+的几何异构体种数有(不考虑光学异构)几种
| |
| [ ] | |
A. |
2种 |
B. |
3种 |
C. |
4种 |
D. |
6种 |
|
2005年9月始,“禽流感”在全球部分地区爆发,引起了人们继“非典型性肺炎”之后的世界范围内的恐慌.做好环境消毒是预防“禽流感”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好.已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-,下列有关说法中正确的是 | |
| [ ] | |
A. |
ClO2的分子结构呈V型,属非极性分子 |
B. |
ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以1mol物质得电子的数目表示)是Cl2的5倍 |
C. |
ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
D. |
常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
|
原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关,下列说法中不正确的是 | |
| [ ] | |
A. |
由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e-=Al3+ |
B. |
由Mg、Al、NaOH溶液组成原电池,其负极反应式为: Al-3e-+4OH-=AlO2-+2H2O |
C. |
由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
D. |
由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e-=Cu2+ |
|
共价键的断裂有均裂和异裂两种方式,即:A∶B→A·+B·,均裂:A∶B→A++[∶B]-,异裂,下列化学反应中发生共价键均裂的是 | |
| [ ] | |
A. |
2K+2H2O=2KOH+H2↑ |
B. |
2Na+2C2H5OH→2C2H5ONa+H2↑ |
C. |
Na2CO3+H2O |
D. |
CH3COOH+C2H5OH |
|
简单原子的原子结构可用右下图表示方法形象表示:其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的是
| |
| [ ] | |
A. |
①②③互为同位素 |
B. |
①②③互为同素异形体 |
C. |
①②③是三种化学性质不同的粒子 |
D. |
①②③具有相同的质量数 |
|
已知NaCl的摩尔质量为Mg·mol-1,食盐晶体的密度为ρg·cm-3,若右图中Na+与最邻近的Cl-的核间距离为acm,那么阿伏加德罗常数的值可表示为
| |
| [ ] | |
A. |
2Ma3ρ |
B. |
M/a3ρ |
C. |
2M/a3ρ |
D. |
M/2a3ρ |
|
设NA为阿伏加德罗常数,下列叙述正确的是 | |
| [ ] | |
A. |
1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒 |
B. |
1molH2O2与MnO2充分反应转移2NA个电子 |
C. |
将标准状况下,22.4LH2和4gHe均含有NA个分子 |
D. |
常温常压下,lmolNO2气体与水反应生成NA个NO3- |