|
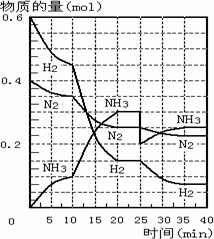
500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是
| |
| [ ] | |
A. |
反应开始到第一次平衡时,N2的平均反应速率为0.005mol/(L·min) |
B. |
从曲线变化可以看出,反应进行到10min至 20min钟时可能是使用了催化剂 |
C. |
从曲线变化可以看出,反应进行至25min钟时,分离出0.1mol的氨气 |
D. |
在25min钟时平衡正向移动但达到新平衡后 NH3的体积分数比原平衡小 |
|
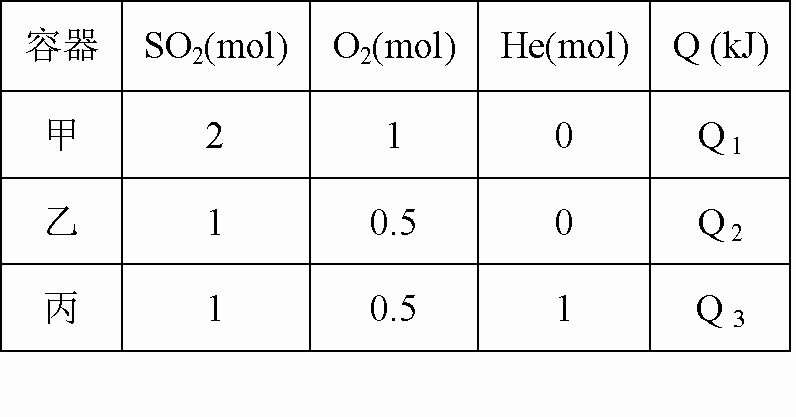
在一定条件下化学反应:2SO2(g) + O2(g)
根据以上数据,下列叙述不正确的是 | |
| [ ] | |
A. |
Q1<197 |
B. |
Q2 =Q3 |
C. |
C、Q1=2Q2 |
D. |
Q1>2Q2 |
|
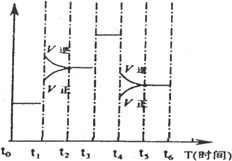
右图表示反应N2(g)+3H2(g) ?2NH3(g);△H<0在某一时间段中反应速率与反应过程的曲线关系图,则氨的百分含量最低的一段时间是
| |
| [ ] | |
A. |
to-t1 |
B. |
t2-t3 |
C. |
3 -t4 |
D. |
t5-t6 |
|
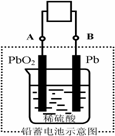
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为Pb+PbO2+4H++2SO42-
| |
| [ ] | |
A. |
放电时:电流方向由B到A |
B. |
放电时:正极反应是Pb-2e-+SO42- |
C. |
充电时:铅蓄电池的负极应与充电器电源的正极相连 |
D. |
充电时:阳极反应是PbSO4-2e-+2H2O |
|
下列叙述不正确的是 | |
| [ ] | |
A. |
原子晶体中原子间平均距离越小,熔、沸点越高 |
B. |
在水溶液中能电离出自由移动的离子的晶体不一定是离子晶体 |
C. |
SnH4、GeH4、SiH4、CH4四种物质的熔点依次降低 |
D. |
水加热到很高的温度都难以分解,是因为水分子之间存在着氢键 |
|
某温度下,在一容积可变的容器中,反应2A(g)+B(g) | |
| [ ] | |
A. |
均减半 |
B. |
均加倍 |
C. |
均增加1 mol |
D. |
均减少1 mol |
|
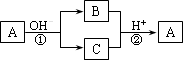
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如下的转化关系(部分产物及反应条件已略去):
下列判断正确的是 | |
| [ ] | |
A. |
X元素可能为Al |
B. |
X元素一定为非金属元素 |
C. |
反应①和②互为可逆反应 |
D. |
反应①、②不一定为氧化还原反应 |
|
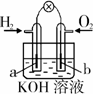
燃料电池是目前电池研究的热点之一.现有某课外小组自制的氢氧燃料电池,如右图所示,a、b均为惰性电极.下列叙述不正确的是
| |
| [ ] | |
A. |
a极是负极,该电极上发生氧化反应 |
B. |
b极反应是O |
C. |
总反应方程式为2H |
D. |
氢氧燃料电池是一种具有应用前景的绿色电源 |
|
下列关于晶体的说法一定正确的是
| |
| [ ] | |
A. |
第ⅠA碱金属元素与ⅦA元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同 |
B. |
晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子 |
C. |
离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键 |
D. |
C60晶体(其结构模型如上图)中每个C60分子周围与它距离最近且等距离的C60分子有12个 |
|
100℃时,将0.1molN2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ①烧瓶内气体的颜色不再加深,②N2O4 的消耗速率与NO2的生成速率之比为1∶2,③NO2的生成速率与NO2消耗速率相等,④NO2的物质的量浓度不变,⑤烧瓶内气体的质量不再变化,⑥烧瓶内气体的压强不再变化,⑦烧瓶内气体的密度不再变化,⑧烧瓶内气体的平均相对分子质量不再变化 | |
| [ ] | |
A. |
②⑤⑦ |
B. |
①③④⑥⑧ |
C. |
只有③ |
D. |
只有⑤ |