|
0.02 mol L-1的HCN溶液与0.02 mol L-1的NaCN溶液等体积混合,测得溶液中c(CN-)<c(Na+),则下列关系中不正确的是 | |
| [ ] | |
A. |
c(Na+)>c(CN-)>c(OH-)>c(H+) |
B. |
c(HCN)+c(CN-)=0.02 mol L-1 |
C. |
c(CN-)c(HCN) |
D. |
c(Na+)+c(H+)=c(CN-)+c(OH-) |
|
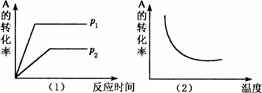
对于可逆反应:mA(g)+nB(g)
| |
| [ ] | |
A. |
△H>0,m+n>x |
B. |
△H>0,m+n<x |
C. |
△H<0,m+n<x |
D. |
△H<0,m+n>x |
|
在一定条件下发生反应:3 A(g)+2 B(g) | |
| [ ] | |
A. |
x=3 |
B. |
B的转化率为20% |
C. |
达到平衡时A的浓度为1.4 mol L-1 |
D. |
平衡时气体压强是原来的0.94倍 |
|
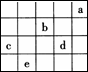
图中a、b、c、d、e为周期表前4周期的一部分元素,下列叙述正确的是
| |
| [ ] | |
A. |
b元素除0价外,只有一种化合价 |
B. |
五种元素中,c元素的性质最稳定 |
C. |
b、d气态氢化物溶于水,溶液的酸性:b>d |
D. |
e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐 |
|
电子层数相同的三种短周期元素X、Y、Z,已知其最高价氧化物对应的水化物的酸性强弱为:HXO4>H2YO4>H3ZO4,则下列判断错误的是 | |
| [ ] | |
A. |
原子半径:X>Y>Z |
B. |
气态氢化物稳定性:HX>H2Y>ZH3 |
C. |
非金属性:X>Y>Z |
D. |
气态氢化物的水溶液的酸性:HX>H2Y>ZH3 |
|
把100 g密度为1.22 g cm-3的NaOH溶液蒸发浓缩,当余下溶液50 mL时其物质的量浓度为8 mol L-1(蒸发浓缩时无固体析出),则原溶液的浓度为①160 g L-1②3.28 mol L-1③4.88 mol L-1④16% | |
| [ ] | |
A. |
① |
B. |
②④ |
C. |
③④ |
D. |
①③ |
|
设NA为阿伏加德罗常数,下列有关叙述不正确的是 | |
| [ ] | |
A. |
常温常压下,1 mol碳烯(∶CH2)所含电子总数为8NA |
B. |
在标准状况下,V L水中含有的氧原子个数为 |
C. |
1 L pH=1的水溶液中水合氢离子数为0.1 NA |
D. |
1 mol OH-在电解过程中被氧化,提供电子的数目为VA |
|
已知:①C(s)+ | |
| [ ] | |
A. |
-283.01 kJ mol-1 |
B. |
+172.51 kJ mol-1 |
C. |
+283.01 kJ mol-1 |
D. |
+504.00 kJ mol-1 |