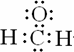|
下列叙述错误的是 | |
| [ ] | |
A. |
硝酸银溶液通常保存在棕色试剂瓶中,因为硝酸银见光易分解 |
B. |
乙醇的沸点比甲醚(CH3-O-CH3)高,主要原因是乙醇分子间作用力更大 |
C. |
反应AgCl+Br-→AgBr+Cl-能在水溶液中进行,是因为AgBr比AgCl更难溶于水 |
D. |
常温下浓硫酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应 |
|
下列物质的制备,符合工业生产实际的是 | |
| [ ] | |
A. |
电解饱和氯化钠溶液制备金属钠 |
B. |
将氨气与二氧化碳先后通入饱和食盐水中,生成碳酸氢钠沉淀,再生成纯碱 |
C. |
将氢气和氯气混合后点燃,产物用浓盐酸吸收制备盐酸 |
D. |
将SO2和O2的混合气加压后,通过接触室制备SO3 |
|
下列有关物质性质和应用的因果关系正确的是 | |
| [ ] | |
A. |
二氧化锰具有强氧化性,能将双氧水氧化为氧气 |
B. |
浓硫酸具有较强酸性,能使Cu转化为Cu2+ |
C. |
炭具有还原性,一定条件下能将二氧化硅还原为硅 |
D. |
二氧化硫具有漂白性,所以与氯水混合使用效果更好 |
|
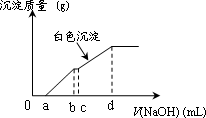
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH(aq),生成沉淀的质量与滴入NaOH(aq)的体积关系如下图.原混合溶液中MgCl2与FeCl3的物质的量之比为
| |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
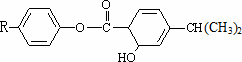
有机物M的结构如下图所示(R为烷烃基),关于M的正确判断是
| |
| [ ] | |
A. |
M难溶于水,也不能与水反应 |
B. |
M能使酸性KMnO4(aq)褪色、使FeCl3(aq)显紫色 |
C. |
M能发生酯化、氧化和加聚反应 |
D. |
常温下1 mol M最多能与3 mol NaOH(aq)反应 |
|
灰锡(以粉末状态存在)和白锡是锡的两种同素异形体.已知: ①Sn(s、白)+2HCl(aq)→SnCl2(aq)+H2(g)+Q1 ②Sn(s、灰)+2HCl(aq)→SnCl2(aq)+H2(g)+Q2 ③Sn(s、灰) 根据以上信息推断正确的是 | |
| [ ] | |
A. |
灰锡、白锡的互相转化是可逆反应 |
B. |
常温下锡以灰锡状态存在 |
C. |
反应中的能量变化:Q1<Q2 |
D. |
长期处于13.2℃以下,锡制器皿会自行毁坏 |
|
在化学能与电能的转化过程中,下列叙述正确的是 | |
| [ ] | |
A. |
电解饱和食盐水时,阳极得到Cl2和NaOH(aq) |
B. |
教材所示的铜-锌原电池在工作时,Zn2+向铜片附近迁移 |
C. |
电镀时,电镀槽里的负极材料发生氧化反应 |
D. |
原电池与电解池连接后,电子从原电池负极流向电解池阳极 |