|
下列对检验方法或现象描述错误的是 | |
| [ ] | |
A. |
苯中是否混有苯酚,可用加溴水是否产生白色沉淀进行检验 |
B. |
乙醛中是否混有乙醇,可用加入金属钠是否产生气体进行检验 |
C. |
乙醇中是否混有水,可用加硫酸铜粉末是否变蓝进行检验 |
D. |
乙酸乙酯是否混有乙酸,可用加石蕊试液是否变红进行检验 |
|
浓硫酸的性质有:①酸性、②强氧化性、③脱水性、④难挥发性等.乙醇、溴化钠和浓硫酸混合共热制备溴乙烷时,会有多个副反应发生,此过程中浓硫酸显示的性质是 | |
| [ ] | |
A. |
①②③④ |
B. |
①和② |
C. |
只有① |
D. |
①和④ |
|
常温下,在等体积①pH=0的硫酸、②0.01 mol/L NaOH溶液、③pH=10的纯碱溶液、④pH=5的NH4Cl溶液中,水电离程度的大小顺序是 | |
| [ ] | |
A. |
①>②>③>④ |
B. |
②>①>④>③ |
C. |
③>④>②>① |
D. |
④>③>②>① |
|
25℃,加水稀释10 mL pH=11的氨水,下列判断正确的是 | |
| [ ] | |
A. |
原氨水的浓度=10-3 mol/L |
B. |
氨水的电离程度增大,溶液中所有离子的浓度均减小 |
C. |
溶液中 |
D. |
再加入10 mL pH=3的盐酸,混合液pH=7 |
|
已知镓(31Ga)和溴(35Br)是第四周期的主族元素.下列分析正确的是 | |
| [ ] | |
A. |
与镓同主族且相邻周期的元素,其原子序数为23或49 |
B. |
与镓同周期且相邻主族的元素,其原子序数为30或32 |
C. |
原子半径:Br>Ga>Cl>Al |
D. |
碱性:KOH>Ga(OH)3>Al(OH)3 |
|
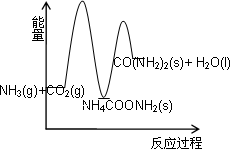
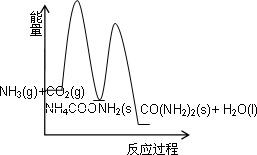
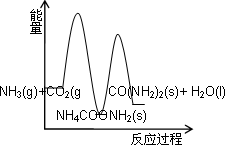
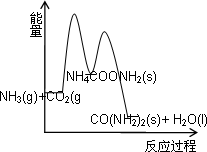
合成尿素的反应2NH3(g)+CO2(g)→CO(NH2)2(s)(尿素)+H2O(l)+Q分两步进行: ①2NH3(g)+CO2(g)→NH4COONH2(s)+Q1, ②NH4COONH2(s)→CO(NH2)2(s)+H2O(l)-Q2. 下列示意图中,能正确表示合成尿素过程中能量变化的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
元素的原子结构决定其性质和在周期表中的位置.下列叙述正确的是 | |
| [ ] | |
A. |
多电子原子中,在离核较近的区域内运动的电子能量较高 |
B. |
原子核外电子的数目越多,电子的运动状态就越多 |
C. |
轨道表示式,是对原子核外电子运动状态最完美的描述 |
D. |
所有元素原子的最外层电子数都等于该元素的最高化合价 |
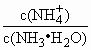 的增大
的增大