|
设nA为阿伏加德罗常数的数值,下列说法正确的是 | |
| [ ] | |
A. |
常温常压下,8 g O2含有4nA个电子 |
B. |
1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
C. |
标准状况下,22.4 L盐酸含有nA个HCl分子 |
D. |
1 mol Na被完全氧化生成Na2O2,失去个2nA电子 |
|
下列有关电解质溶液的说法正确的是 | |
| [ ] | |
A. |
在蒸馏水中滴加浓H2SO4,KW不变 |
B. |
CaCO3难溶于稀硫酸,也难溶于醋酸 |
C. |
在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
D. |
NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
|
下列实验误差分析错误的是 | |
| [ ] | |
A. |
用湿润的PH试纸测稀碱液的PH,测定值偏小 |
B. |
用容量瓶配置溶液,定容时俯视刻度线,所配溶液浓度偏小 |
C. |
滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 |
D. |
测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏小 |
|
下列有关元素的性质及其底边规律正确的是 | |
| [ ] | |
A. |
ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物 |
B. |
最高第二周期元素从左到右,正价从+1递增到+7 |
C. |
同主族元素的简单阴离子还原性越强,水解程度越大 |
D. |
同周期金属元素的化合价越高,其原子失电子能力越强 |
|
运用有关概念判断下列叙述正确的是 | |
| [ ] | |
A. |
1 mol H2燃烧放出的热量为H2的燃烧热 |
B. |
Na2SO3和H2O2的反应为氧化还原反应 |
C. |
|
D. |
BaSO4的水溶液不导电,故BaSO4是弱电解质 |
|
我国科学家研制出一中催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2 | |
| [ ] | |
A. |
该反应为吸热反应 |
B. |
CO2分子中的化学键为非极性键 |
C. |
HCHO分子中既含α键又含π键 |
D. |
没生成1.8 gH2O消耗2.24 L O2 |
|
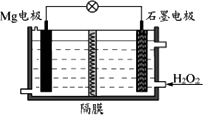
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液,示意图如下.该电池工作时,下列说法正确的是
| |
| [ ] | |
A. |
Mg电极是该电池的正极 |
B. |
H2O2在石墨电极上发生氧化反应 |
C. |
石墨电极附近溶液的pH增大 |
D. |
溶液中Cl-向正极移动 |