|
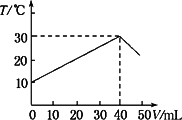
向盛有50 mL 1.00 mol·L-1 HCl溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列不正确的是
| |
| [ ] | |
A. |
该实验表明化学能可以转化为热能 |
B. |
NaOH溶液的浓度大于1.00 mol/L |
C. |
V=50 mL时,混合液的pH>7 |
D. |
该实验表明有水生成的反应都是放热反应 |
|
在一定温度下,反应 | |
| [ ] | |
A. |
5% |
B. |
17% |
C. |
25% |
D. |
33% |
|
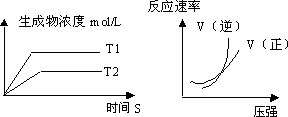
可逆反应aA(g)+bB(g)
| |
| [ ] | |
A. |
a+b>c+d;T1>T2;Q>O |
B. |
a+b>c+d;T1<T2;Q<O |
C. |
a+b<c+d;T1>T2;Q>O |
D. |
a+b>c+d;T1>T2;Q<O |
|
铁和氧化铁的混合物共a mol,加盐酸后固体全部溶解,共收集到b mol氢气,且向反应后的溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为 | |
| [ ] | |
A. |
|
B. |
(a-b)mol |
C. |
|
D. |
(a+b)mol |
|
对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,下列说法正确的是 | |
| [ ] | |
A. |
只有硫酸铜作氧化剂 |
B. |
SO |
C. |
被氧化的硫与被还原的硫的质量比为3∶7 |
D. |
1 mol硫酸铜可以氧化 |
|
在100 mL混合溶液中,HNO3和H2SO4的物质的量浓度分别为0.4 mol/L和0.1 mol/L,向该混合液中加入1.92 g铜,加热后,所得溶液中Cu2+的浓度是 | |
| [ ] | |
A. |
0.15 mol/L |
B. |
0.225 mol/L |
C. |
0.35 mol/L |
D. |
0.45 mol/L |
|
有下列两个反应,当温度降低时,反应a平衡右移,反应b平衡左移. a、C2H2(g)+H2(g) b、2CH4(g) 根据上述变化,判断以下几个热化学方程式: C(s)+2H2(g) 2C(s)+H2(g) 2C(s)+2H2(g) 其中2Q1、Q2、Q3从大到小的顺序是 | |
| [ ] | |
A. |
2Q1>Q3>Q2 |
B. |
Q3>2Q1>Q2 |
C. |
Q2>Q3>2Q1 |
D. |
Q3>2Q1>Q2 |
|
三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如下图所示,已知其燃烧热△H=-3677 kJ/mol(磷元素被氧化为P4O10),下列有关P4S3的说法中不正确的是
| |
| [ ] | |
A. |
分子中每个原子最外层均达到8电子稳定结构 |
B. |
P4S3中磷元素为+3价 |
C. |
热化学方程式为P4S3(s)+8O2(g)=P4O10(s)+3SO2(g);△H=-3677 kJ/mol |
D. |
分子中存在极性键与非极性键 |
|
甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液.向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成气体的体积比为1∶2,求所加入的铝粉质量为 | |
| [ ] | |
A. |
5.4 g |
B. |
3.6 g |
C. |
2.7 g |
D. |
1.8 g |