|
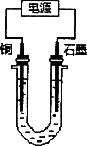
已知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量.该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用图所示装置电解,其中某电极增重a g,另一电极上产生标准状况下的气体V mL.下列说法正确的是
| |
| [ ] | |
A. |
黑色粉末X是铁粉 |
B. |
铜电极连接电源正极 |
C. |
石墨电极上发生的反应是4OH--4e-=O2↑+2H2O |
D. |
铜的相对原子质量的计算式是 |
|
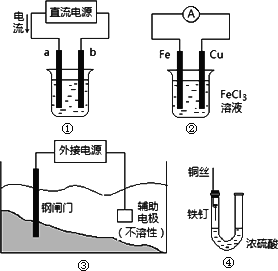
关于下列各装置图的叙述中,不正确的是
| |
| [ ] | |
A. |
用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
B. |
装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
C. |
装置③中钢闸门应与外接电源的负极相连 |
D. |
装置④中的铁钉几乎没被腐蚀 |
|
下列叙述中,正确的是 | |
| [ ] | |
A. |
在船舶的外壳装上铜块可防止其发生电化学腐蚀 |
B. |
MnO2、FeCl3和CuSO4都可加快H2O2的分解速率 |
C. |
FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
D. |
用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg |
|
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是 | |
| [ ] | |
A. |
既不是氧化剂也不是还原剂 |
B. |
是氧化剂 |
C. |
是还原剂 |
D. |
既是氧化剂又是还原剂 |
|
有甲、乙两种水的乙醇溶液,甲中水的质量分数为25%,乙中水的质量分数为15%,将甲、乙两种溶液各取100 mL混合,则所得溶液中水的质量分数w为 | |
| [ ] | |
A. |
w>0.80 |
B. |
0.20<w<0.80 |
C. |
w<0.20 |
D. |
无法确定 |
|
将51.2 gCu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/LNaOH溶液完全吸收,生成的盐溶液中NaNO3的物质的量为(已知:2NO2+2NaOH=NaNO3+NaNO2+H2O;NO+NO2+2NaOH=2NaNO2+H2O) | |
| [ ] | |
A. |
0.2 mol |
B. |
0.4 mol |
C. |
0.6 mol |
D. |
0.8 mol |
|
纯净的氯化钠是不潮解的,但粗盐很容易潮解,这主要是因为其中含有杂质MgCl2的缘故.为得到纯净的氯化钠,有人设计了一个实验:把买来的粗盐放入纯氯化钠饱和溶液一段时间,过滤,洗涤,可得纯净的氯化钠晶体.则下列说法中,正确的是 | |
| [ ] | |
A. |
设计实验的根据是NaCl的溶解平衡 |
B. |
设计实验的根据是MgCl2比NaCl易溶于水 |
C. |
在整个过程中NaCl饱和溶液浓度会变大(温度不变) |
D. |
粗盐的晶粒大一些有利于提纯 |
|
标准状况下VL氨气溶解在1 L水中(水的密度近似为1 g/ml),所得溶液的密度为p g/ml,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是 | |
| [ ] | |
A. |
p=(17 V+22400)/(22.4+22.4 V) |
B. |
ω=17c/(1000ρ) |
C. |
ω=17 V/(17 V+22400) |
D. |
C=1000 Vρ/(17 V+22400) |
|
下列叙述正确的是 | |
| [ ] | |
A. |
在醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
B. |
在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
C. |
1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-8 mol/L盐酸的pH=8.0 |
D. |
常温下,若1 mLpH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7则NaOH溶液的pH=11 |