|
室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是 | |
| [ ] | |
A. |
0.1 mol/L的盐酸和0.1 mol/L的氢氧化钠溶液 |
B. |
0.1 mol/L的盐酸和0.1 mol/L的氢氧化钡溶液 |
C. |
pH=4的醋酸溶液和pH=10的氢氧化钠溶液 |
D. |
pH=4的盐酸和pH=10的氨水 |
|
根据相关化学原理,下列判断正确的是 | |
| [ ] | |
A. |
若X是原子晶体,Y是分子晶体,则熔点:X<Y |
B. |
若A2+2D-→2A-+D2,则氧化性:D2>A2 |
C. |
若R2-和M+的电子层结构相同,则原子序数:R>M |
D. |
若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的碱性:NaA<NaB |
|
将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是 | |
| [ ] | |
A. |
反应速率:两者相同 |
B. |
消耗硝酸的物质的量:前者多,后者少 |
C. |
反应生成气体的颜色:前者浅,后者深 |
D. |
反应中转移的电子总数:前者多,后者少 |
|
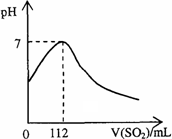
在标准状况下,向100 mL氢硫酸溶液中通人二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为
| |
| [ ] | |
A. |
0.5 mol/L |
B. |
0.05 mol/L |
C. |
1 mol/L |
D. |
0.1 mol/L |
|
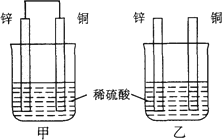
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
| |
| [ ] | |
A. |
两烧杯中铜片表面均无气泡产生 |
B. |
甲中铜片是正极,乙中铜片是负极 |
C. |
两烧杯中溶液的pH均增大 |
D. |
产生气泡的速度甲比乙慢 |
|
二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命.二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH.下列有关二甘醇的叙述正确的是 | |
| [ ] | |
A. |
不能发生消去反应 |
B. |
能发生取代反应 |
C. |
能溶于水,不溶于乙醇 |
D. |
符合通式CnH2nO3 |
|
某非金属单质A和氧气发生化合反应生成B.B为气体,其体积是反应掉氧气体积的两倍(同温同压).以下对B分子组成的推测一定正确的 | |
| [ ] | |
A. |
有1个氧原子 |
B. |
有2个氧原子 |
C. |
有1个A原子 |
D. |
有2个A原子 |