|
在常温下,发生下列几种反应: ①16H++10Z-+2XO4-=2X2++5Z2+8H2O ②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z- 根据上述反应,判断下列结论中错误的是: | |
| [ ] | |
A. |
溶液中可发生:Z2+2A2+=2A3++2Z- |
B. |
Z2在①、③反应中为还原剂 |
C. |
氧化性强弱的顺序为:XO4->Z2>B2>A3+ |
D. |
X2+是XO4-的还原产物 |
|
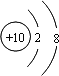
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素 | |
| [ ] | |
A. |
在自然界中只以化合态的形式存在 |
B. |
单质常用作半导体材料和光导纤维 |
C. |
最高价氧化物不与酸反应 |
D. |
气态氢化物比甲烷稳定 |
|
下列说法正确的是 | |
| [ ] | |
A. |
根据反应5Fe2++MnO4-+8H+ |
B. |
根据反应3Fe+8HNO3 |
C. |
根据反应CuSO4+H2S |
D. |
根据反应H3PO3+2NaOH(足量)=Na2HPO3+2H2O可知:H3PO3属于三元酸 |
|
下列说法中不正确的有 ①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂; ②光照氯水有气泡逸出,该气体是Cl2; ③燃煤时加入适量石灰石,可减少废气中SO2的量; ④pH在5.6~7.0之间的降水通常称为酸雨; ⑤室温下浓硫酸与铜片不会发生剧烈的化学反应,原因是铜被钝化. ⑥氯气易液化,液氯可以保存在钢瓶中; ⑦常温下浓硫酸可以用铝制容器盛放; ⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤 | |
| [ ] | |
A. |
2个 |
B. |
3个 |
C. |
4个 |
D. |
5个 |
|
在200 mL某硫酸盐溶液中含有1.5 NA个硫酸根离子(NA表示阿伏加德罗常数),同时含有NA个金属阳离子,则该硫酸盐的物质的量浓度为 | |
| [ ] | |
A. |
1 mol·L-1 |
B. |
2.5 mol·L-1 |
C. |
5 mol·L-1 |
D. |
2 mol·L-1 |
|
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关.下列各组物质: ①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液.由于浓度不同而能发生不同氧化还原反应的是 | |
| [ ] | |
A. |
①③ |
B. |
③④ |
C. |
①② |
D. |
①③④ |
|
古诗词是古人为我们留下的宝贵精神财富,下列诗句不涉及氧化还原反应的是 | |
| [ ] | |
A. |
野火烧不尽,春风吹又生 |
B. |
春蚕到死丝方尽,蜡炬成灰泪始干 |
C. |
粉身碎骨浑不怕,要留清白在人间 |
D. |
爆竹一声一岁除,春风送暖入屠苏 |
|
下列有关物质的性质及其应用均正确的是 | |
| [ ] | |
A. |
NH3溶于水后显碱性,在FeC13饱和溶液中通入适量NH3可制取Fe(OH)3胶体 |
B. |
金属有导热性,铝、钠熔点不高,核反应堆内使用液体铝钠合金作载热介质 |
C. |
碳酸钠溶液显碱性,用热的饱和碳酸钠溶液可除去金属表面的矿物油污 |
D. |
次氯酸钠具有强还原性,可用于配制“84”消毒液 |