|
下表为有关化合物的pKsp,pKsp=-lgKsp,某同学设计实验如下: ①向AgNO3溶液中加入适量NaX溶液,得到沉淀AgX; ②向①中加NaY,则沉淀转化为AgY; ③向②中加入Na2Z,沉淀又转化为Ag2Z.则表中a、b、c的大小关系为
| |
| [ ] | |
A. |
a>b>c |
B. |
a<b<c |
C. |
c<a<b |
D. |
a+b=c |
|
有关难溶电解质的溶度积如下: Mg(OH)2(s) Ksp=5.6×10-12(mol/L)3 Cu(OH)2(s) Ksp=2.2×10-20(mol/L)3 向温度一定、有固态Mg(OH)2存在的饱和溶液中加入某物质或溶液,能使Mg(OH)2固体的质量增加的是 | |
| [ ] | |
A. |
CH3COONa的饱和溶液 |
B. |
NH4Cl的饱和溶液 |
C. |
CuCl2的饱和溶液 |
D. |
蒸馏水 |
|
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:Ca(OH)2(s) | |
| [ ] | |
A. |
c(Ca2+)增大 |
B. |
c(Ca2+)不变 |
C. |
c(OH-)增大 |
D. |
c(OH-)减小 |
|
对水垢的主要成分是CaCO3和Mg(OH)2而不是CaCO3和MgCO3的原因解释,其中正确的是 | |
| [ ] | |
A. |
Mg(OH)2的溶度积大于MgCO3的溶度积,且在水中发生了沉淀转化 |
B. |
Mg(OH)2的溶度积小于MgCO3的溶度积,且在水中发生了沉淀转化 |
C. |
MgCO3电离出的CO |
D. |
MgCO3电离出的CO |
|
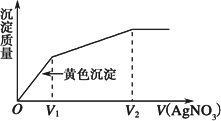
往含I-、Cl-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入的AgNO3溶液体积的关系如图所示,则原溶液中c(I-)、c(Cl-)的比值为
| |
| [ ] | |
A. |
(V2-V1)/V1 |
B. |
V1/V2 |
C. |
V1/(V2-V1) |
D. |
V2/V1 |
|
下列说法正确的是 | |
| [ ] | |
A. |
向饱和食盐水中加入少量的浓盐酸,看不到明显的现象 |
B. |
将硫酸铜溶液与碳酸钠溶液混合,得到的沉淀是以Cu(OH)2为主,说明了在相同条件下Cu(OH)2的溶解度比CuCO3的更小 |
C. |
在0.01 mol/L NaCl溶液中加入少量的AgNO3溶液,有白色沉淀生成,接着向上述溶液中加入足量的浓氨水,白色沉淀不会溶解 |
D. |
CaCO3溶液的导电能力很弱,是因为CaCO3是弱电解质,存在如下电离平衡: CaCO3 |
|
牙齿表面由一层硬的成分为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:Ca5(PO4)3OH(s) | |
| [ ] | |
A. |
饮用纯净水 |
B. |
在牙膏中添加适量的Ca2+或PO |
C. |
在饮用水中添加适量的氟化物 |
D. |
在牙膏中添加适量的氟化物 |
|
已知Ksp(AgCl)=1.8×10-10 (mol/L)2,Ksp(AgI)=1.0×10-16 (mol/L)2.下列关于不溶物之间转化的说法中错误的是 | |
| [ ] | |
A. |
AgCl不溶于水,不能转化为AgI |
B. |
两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 |
C. |
AgI比AgCl更难溶于水,所以AgCl可以转化为AgI |
D. |
常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度必须不低于 |