|
守恒:如质量守恒,电子守恒,电荷守恒等.下列式子符合守恒思想的是 | |
| [ ] | |
A. |
Fe2++Cl2→Fe3++2Cl- |
B. |
4FeS2+11O2→2Fe2O3+8SO2 |
C. |
NH3+H2SO4→(NH4)2SO4 |
D. |
Al3++6OH-→AlO2-+3H2O |
|
把NaHCO3和Na2CO3·10H2O混合物6.56 g溶于水制成100 mL溶液,测得溶液中钠离子的浓度为0.5 mol/L.向该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为 | |
| [ ] | |
A. |
2.93 g |
B. |
5.85 g |
C. |
6.56 g |
D. |
无法确定 |
|
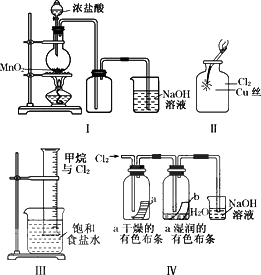
某同学用下列装置制备并检验Cl2的性质:
下列说法正确的是 | |
| [ ] | |
A. |
Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗完 |
B. |
Ⅱ图中:生成蓝色的烟 |
C. |
Ⅲ图中:量筒中发生了加成反应 |
D. |
Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
|
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应.二者比较,相等的是 ①铜片消耗完所需时间; ②反应生成的气体体积(标准状况); ③反应中氧化剂得到的电子总数; ④反应后溶液中铜离子的浓度 | |
| [ ] | |
A. |
①③ |
B. |
②④ |
C. |
③④ |
D. |
只有① |
|
研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下: ①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2 NO2在上述过程中的作用,与H2SO4在下列变化中的作用相似的是 | |
| [ ] | |
A. |
加入少量H2SO4使淀粉水解 |
B. |
碳酸钠与硫酸反应 |
C. |
向铜和双氧水的混合物中加入硫酸 |
D. |
潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
|
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是 | |
| [ ] | |
A. |
2Na218O2+2H2O |
B. |
NH4Cl+2H2O |
C. |
2KMnO4+5H218O2+3H2SO4 |
D. |
K37ClO3+6HCl |
|
已知:2KMnO4+16HCl K2Cr2O7+14HCl 其中,KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6 mol/L)反应,MnO2需和浓盐酸(>8 mol/L)反应.根据以上信息,下列结论中不正确的是 | |
| [ ] | |
A. |
上述反应既属于氧化还原反应,又属于离子反应 |
B. |
生成1 mol Cl2转移电子数均为2NA |
C. |
盐酸浓度越大,Cl-的还原性越强 |
D. |
氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 |
|
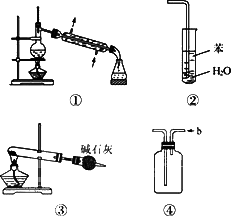
下列关于各实验装置图的叙述中,正确的是
| |
| [ ] | |
A. |
装置①常用于分离互不相溶的液体混合物 |
B. |
装置②可用于吸收NH3,并防止倒吸 |
C. |
以NH4HCO3为原料,装置③可用于实验室制备少量NH3 |
D. |
装置④b口进气可收集Cl2、NO等气体 |
|
下列解释原理的表达式中,不正确的是 | |
| [ ] | |
A. |
镁的冶炼:MgCl2(熔融) |
B. |
用热的纯碱溶液清洗油污:CO |
C. |
用Na2CO3溶液处理水垢中的CaSO4:CaSO4(s)+CO |
D. |
用氢氟酸刻蚀玻璃:4HF+SiO2=SiF4↑+2H2O |