|
下列叙述正确的是 | |
| [ ] | |
A. |
Li在氧气中燃烧主要生成Li2O2 |
B. |
将SO2通入BaCl2溶液可生成BaSO3沉淀 |
C. |
将CO2通入次氯酸钙溶液可生成次氯酸 |
D. |
将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
|
有关①100 ml 0.1 mol/L NaHCO3、②100 ml 0.1 mol/L Na2CO3两种溶液的叙述不正确的是 | |
| [ ] | |
A. |
溶液中水电离出的H+个数:②>① |
B. |
溶液中阴离子的物质的量浓度之和:②>① |
C. |
①溶液中:c(CO |
D. |
②溶液中:c(HCO |
|
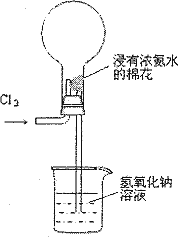
下图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是
| |
| [ ] | |
A. |
烧瓶中立即出现白烟 |
B. |
烧瓶中立即出现红棕色 |
C. |
烧瓶中发生的反应表明常温下氨气有还原性 |
D. |
烧杯中的溶液是为了吸收有害气体 |
|
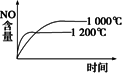
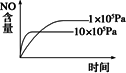
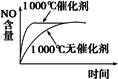
已知:4NH3(g)+5O2(g) 4NO(g)+6H2O(g);ΔH=-1025 KJ/mol,该反应是一个可逆反应.若反应物起始物质的量相同,下列关于该反应的示意图不正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是 | |
| [ ] | |
A. |
2.0 mol/L |
B. |
1.5 mol/L |
C. |
0.18 mol/L |
D. |
0.24 mol/L |
|
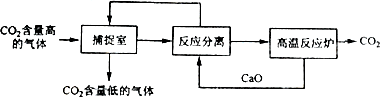
“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用.如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出).
下列有关该方法的叙述中正确的是 | |
| [ ] | |
A. |
能耗小是该方法的一大优点 |
B. |
整个过程中,只有一种物质可以循环利用 |
C. |
“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
D. |
该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品 |
|
下列有关物质的性质和该性质的应用均正确的是 | |
| [ ] | |
A. |
常温下浓硫酸能是铝发生钝化,可在常温下用铝制贮藏贮运浓硫酸 |
B. |
二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
C. |
二氧化氯具有还原性,可用于自来水的杀菌消毒 |
D. |
铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
|
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素 | |
| [ ] | |
A. |
在自然界中只以化合态的形式存在 |
B. |
单质常用作半导体材料和光导纤维 |
C. |
最高价氧化物不与酸反应 |
D. |
气态氢化物比甲烷稳定 |