|
下列各组物质的分类正确的是 ①混合物:氯水、氨水、水玻璃、水银 ②电解质:明矾、冰醋酸、石膏、纯碱 ③同位素:1H+、2H+、3H+ ④同素异形体:C60、C80、金刚石、石墨 ⑤弱电解质:HF、SO2、NH3、H2O | |
| [ ] | |
A. |
②④ |
B. |
②③④ |
C. |
②④⑤ |
D. |
全部正确 |
|
已知热化学方程式: 2CO2(g)+O2(g) 下列说法正确的是 | |
| [ ] | |
A. |
相同条件下,2 mol SO2(g)和1 mol O2(g)所具有的能量小于2 mol SO3(g)所具有的能量 |
B. |
将2 mol SO2(g)和1 mol O2(g)置于一密闭容器中充分反应后,放出热量为QkJ |
C. |
增大压强或升高温度,该平衡都向逆反应方向移动 |
D. |
如将一定量SO2(g)和O2(g)置于某密闭容器中充分反应后放热QkJ,则此过程中有2 mol SO2(g)被氧化 |
|
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) | |
| [ ] | |
A. |
以X浓度变化表示的反应速率为0.001 mol·L-1·s-1 |
B. |
其它条件不变,将容器体积变为20 L,Z的平衡浓度变为原来的 |
C. |
其它条件不变,若增大压强,则物质Y的转化率减小 |
D. |
其它条件不变,若升高温度,X的体积分数增大,则该反应的ΔH>0 |
|
在中和滴定中,下列操作或说法不正确的是 | |
| [ ] | |
A. |
使用滴定管时,洗涤后必须用待装液润洗2~3次 |
B. |
盛装准确量取的待测液的锥形瓶用待测液润洗2~3次 |
C. |
酸式滴定管不能盛装碱液,碱式滴定管不能盛装酸液或强氧化性溶液 |
D. |
滴定终点时,若不慎滴入过量标准溶液,可用装有待测液的滴定管再滴入一定量进行调整 |
|
下列有关沉淀溶解平衡的说法正确的是 | |
| [ ] | |
A. |
KSP(AB2)小于KSP(CD),则物质AB2的溶解度一定小于物质CD的溶解度 |
B. |
在氯化银的沉淀溶解平衡体系中,加入蒸馏水,氯化银的KSP增大 |
C. |
在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 |
D. |
在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,溶解平衡不移动 |
|
氢氧燃料电池以氢气作还原剂,氧气作氧化剂,电极为多孔镍,电解质溶液为30%的氢氧化钾溶液.以下有数种说法: ①负极反应为O2+2H2O+4e-→4OH- ②负极反应为2H2+4OH-→4H2O+4e- ③电池工作时正极区pH升高,负极区pH下降 ④电池工作时溶液中的阴离子移向正极 正确的组合是 | |
| [ ] | |
A. |
②③ |
B. |
②④ |
C. |
①③④ |
D. |
①④ |
|
下面是从某中学化学教材中摘录的内容,其中表述得不够科学严密的是 | |
| [ ] | |
A. |
有电子转移(得失或偏移)的化学反应都是氧化还原反应 |
B. |
元素化合价的数值,与原子的电子层结构特别是最外层电子数有关 |
C. |
电子是在原子核外距核由近及远、能量由低到高的不同电子层上分层排布的 |
D. |
将两种带相反电荷的胶体混合,也能发生聚沉 |
|
2.1 g平均相对分子质量为7.2的CO和H2组成的混合气体与足量的O2充分反应后,立即通入足量的Na2O2固体中,充分反应,固体的质量增加 | |
| [ ] | |
A. |
2.1 g |
B. |
7.2 g |
C. |
9.3 g |
D. |
以上答案均不正确 |
|
NA代表阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
1 L 1 mol·L-1的Na2SO4溶液中含有Na+的个数为NA |
B. |
2 g氢气所含氢原子数目为NA |
C. |
在常温常压下,11.2 L氮气所含的原子数目为NA |
D. |
1.7 g氨气所含分子数目为0.1NA |
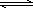 2CO3(g)ΔH=-QkJ·mol-1(Q>0).
2CO3(g)ΔH=-QkJ·mol-1(Q>0).
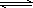 Z(g),经60 s达到平衡,生成0.3 mol Z.下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z.下列说法正确的是