|
已知0.01 mol/l二元酸H2A溶液的PH=4,下列说法正确的是 | |
| [ ] | |
A. |
在Na2A,NaHA两种溶液中,离子种类不相同 |
B. |
在溶质的物质的量相等的Na2A,NaHA两种溶液中,阴离子总数相等 |
C. |
在NaHA溶液中一定有c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-) |
D. |
在Na2A溶液中一定有C(H+)+c(HA-)=c(OH-)-2C(H2A) |
|
室温下某无色透明溶液中由水电离出的H+和OH-浓度的乘积为1×10-24,则此溶液中可能大量共存的离子组为 | |
| [ ] | |
A. |
HCO3-、Al3+、Na+、SO42- |
B. |
I-、NO3-、K+、NH4+ |
C. |
MnO4-、Cl-、SO42-、K+ |
D. |
SiO32-、OH-、SO32-、Na+、Cl- |
|
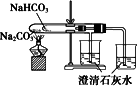
现有H2SO4、BaCl2、K2CO3、FeSO4和氯水五种溶液,有如图所示的相互关系,图中每条连线两端的物质可以发生化学反应.下列推断不合理的是
| |
| [ ] | |
A. |
X一定为H2SO4 |
B. |
Y一定为K2CO3 |
C. |
Z可能是氯水 |
D. |
M可能为FeSO4 |
|
在一定条件下,对于反应mA(g)+nB(g)
| |
| [ ] | |
A. |
ΔH<0 ΔS>0 |
B. |
ΔH>0 ΔS<0 |
C. |
ΔH>0 ΔS>0 |
D. |
ΔH<0 ΔS<0 |
|
能正确表示下列反应的离子方程式是 | |
| [ ] | |
A. |
将Fe(OH)3溶于HI溶液中:Fe(OH)3+3H+=Fe3++3H2O |
B. |
NaHCO3溶液水解:HCO3-+H2O |
C. |
用浓硫酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO |
D. |
向 Ba(HCO3)2溶液中加入少量的NaOH溶液Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O |
|
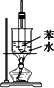
已知NH4CuSO3与足量的2 mol/L硫酸溶液混合微热,产生下列现象: ①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是 | |
| [ ] | |
A. |
反应中硫酸作氧化剂 |
B. |
NH4CuSO3中硫元素被氧化 |
C. |
1 mol NH4CuSO3完全反应转移0.5 mol电子 |
D. |
刺激性气味的气体是氨气 |
|
25℃ 、101 kPa下,反应2N2O5(g)=4NO2(g)+O2(g) ΔH=+56.7 kJ/mol能自发进行的原 | |
| [ ] | |
A. |
是吸热反应 |
B. |
是放热反应 |
C. |
是熵减小的反应 |
D. |
熵增效应大于热效应 |
|
分类是学习和研究化学的一种常用的科学方法.下列6项分类中合理的有几项 ①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等 ②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应 ③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质 ④根据元素原子最外层电子数的多少将元素分为金属和非金属 ⑤根据反应的热效应将化学反应分为放热反应和吸热反应 ⑥根据分散剂的直径大小,分散系可分为溶液、胶体和浊液 | |
| [ ] | |
A. |
1项 |
B. |
2项 |
C. |
3项 |
D. |
4项 |
|
下列各表述正确的是 | |
| [ ] | |
A. |
2NO+2CO=N2+CO2 ΔH<0,该反应不一定能自发进行 |
B. |
甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
C. |
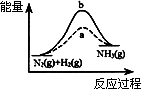
500℃ 、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) |
D. |
图中a曲线表示合成氨使用催化剂时,反应过程中的能量变化
|
 cC(g)+dD(g),C物质的浓度(c%)与温度、压强的关系如图所示,下列判断正确的是
cC(g)+dD(g),C物质的浓度(c%)与温度、压强的关系如图所示,下列判断正确的是