|
已知:CH4(g)+2O2(g) 2H2(g)+O2(g)=2H2O(g) ΔH=-Q2kJ·mol-1 2H2(g)+O2(g)=2H2O(1) ΔH=-Q3kJ·mol-1 常温下,取体积比为3∶2的甲烷和氢气的混合气体33.6 L(标准状况),经完全燃烧后恢复到常温,放出的热量(单位:kJ)为 | |
| [ ] | |
A. |
0.9Qi+0.6Q2 |
B. |
0.6Q1+0.4Q2 |
C. |
0.9Q11+0.3Q3 |
D. |
0.6Q1+0.4Q3 |
|
下列关于热化学反应的描述,正确的是 | |
| [ ] | |
A. |
甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
B. |
500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为(条件略): N2(g)+3H2(g) |
C. |
CO(g)的燃烧热是283.0 kJ·mol-1,则有热化学方程式为:2CO2(g) |
D. |
HC1和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
|
某密闭容器中发生如下反应:X(g)+3Y(g)
| |
| [ ] | |
A. |
t2时加入了催化剂 |
B. |
t3时降低了温度 |
C. |
t3时增大了压强 |
D. |
t4~t5时间内反应物的转化率一定最低 |
|
在由水电离的OH-浓度为2.0×10-1z mol lL的溶液中不可能大量共存的离子组是 | |
| [ ] | |
A. |
K+、MnO4-、Mg2+、NO3- |
B. |
Fe2+、Na+、NO-3、Cu2+ |
C. |
Na+、H+、NO3-、SO2-4 |
D. |
Fe3+、Na+、C1-、SO2-4 |
|
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是 | |
| [ ] | |
A. |
X、M两种元素只能形成XzM型化合物 |
B. |
由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
C. |
X、Y、Z、W的原子半径依次增大 |
D. |
元素W和M的某些单质可作为水处理中的消毒剂 |
|
2003年,IUPAC(国际纯粹与应用化学联合会)推荐原子序数为110的元素的符号为Ds,以纪念该元素的发现地(Darmstadt,德国).下列关于Ds的说法不正确的是 | |
| [ ] | |
A. |
Ds原子的电子层数为7 |
B. |
Ds是超铀元素 |
C. |
Ds原子的质量数为110 |
D. |
Ds为金属元素 |
|
将钠在干燥的空气中形成的氧化物1.4 g溶于水后,可被80 mL 0.5 mol/L盐酸恰好中和,钠的氧化物的成分是 | |
| [ ] | |
A. |
Na2O |
B. |
Na2O与Na2O2 |
C. |
Na2O2 |
D. |
Na2O与Na2O |
|
能正确表示下列反应的离子方程式是 | |
| [ ] | |
A. |
向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+H2O+CO2 |
B. |
向次氯酸钙溶液通入SO2:Ca2++2C1O-十H2O+SO2 |
C. |
氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO3- |
D. |
在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO-3 |
|
下列现象或事实可用同一原理解释的是 | |
| [ ] | |
A. |
在FeC12溶液和Fe(OH)2胶体中加入NaOH溶液均能产生红褐色沉淀 |
B. |
二氧化硅在氢氟酸、氢氧化钠溶液中郡能溶解 |
C. |
次氯酸和二氧化硫都具有漂白作用,能使品红溶液褪色 |
D. |
H2O2溶液中加入MnO2或FeCl3溶液都能增大反应速率 |
|
用NA表示阿伏加德罗常数,下列叙述正确的是 | |
| [ ] | |
A. |
标准状况下,22.4 L H2O含有的分子数为NA |
B. |
常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02 NA |
C. |
通常状况下,NA个CO2分子占有的体积为22.4 L |
D. |
物质的量浓度为1.5 mol 1 L的MgCl2溶液中,含有Cl-数为3NA |
 COz(g)+2Hz0(1) ΔH=-Q1kJ·mol-1
COz(g)+2Hz0(1) ΔH=-Q1kJ·mol-1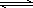 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1 2CO(g)+O2(g) ΔH=+2×283.0 kJ·mol-1
2CO(g)+O2(g) ΔH=+2×283.0 kJ·mol-1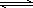 2Z(g);ΔH<O.下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是
2Z(g);ΔH<O.下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是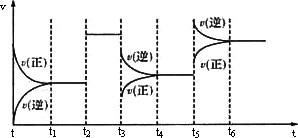
 CaCO3↓+2HC1O
CaCO3↓+2HC1O CaCO3↓+2HC1O
CaCO3↓+2HC1O CaCO3↓+H2O
CaCO3↓+H2O 3Fe3++2H2O+NO↑
3Fe3++2H2O+NO↑