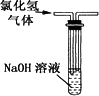
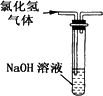
|
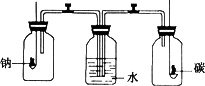
有三个氧化还原反应:①2FeCl3+2KI ②2FeCl2+Cl2 ③2KMnO4+16HCl 若某溶液中有Fe2+、I-和Cl-共存,要氧化除去I-而不影响Fe2+和Cl-,可加入的试剂是 | |
| [ ] | |
A. |
Cl2 |
B. |
KMnO4 |
C. |
FeCl3 |
D. |
HCl |
|
是某学校实验室从化学试剂商店买回的硫酸试剂标签上的内容.据此,下列说法正确的是
| |
| [ ] | |
A. |
该硫酸的物质的量浓度为9.2 mol/L |
B. |
1 mol Zn与足量的该硫酸反应产生2克H2 |
C. |
配制200 ml 4.6 mol/L的稀硫酸需要取该硫酸50 ml |
D. |
该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L |
|
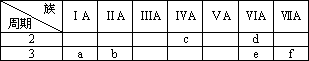
是元素周期表的一部分,有关说法正确的是
| |
| [ ] | |
A. |
e的氢化物比d的氢化物稳定 |
B. |
a、b、e三种元素的原子半径:e>b>a |
C. |
六种元素中,c元素单质的化学性质最活泼 |
D. |
c、e、f的最高价氧化物对应的水化物的酸性依次增强 |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO |
B. |
Ca(HCO3)2+与过量Ca(OH)2溶液反应:Ca2++HCO |
C. |
NaCO3溶液中通入过量CO2:CO |
D. |
CH3COOH溶液与NaOH溶液反应:H++OH-=H2O |
|
氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是 | |
| [ ] | |
A. |
一个D2O分子所含的中子数为8 |
B. |
NH3的结构式为 |
C. |
HCl的电子式为H+[ |
D. |
热稳定性:H2S>HI |
|
航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4 | |
| [ ] | |
A. |
上述反应中,每生成1 mol N2则转移电子6 mol |
B. |
上述反应瞬间产生大量高温气体推动航天飞机飞行 |
C. |
反应从能量变化上说,主要是化学能转变为热能和动能 |
D. |
在反应中高氯酸铵既起氧化剂,又起还原剂作用 |
|
下列说法正确的是 | |
| [ ] | |
A. |
少量SO2通过浓的CaCl2溶液能生成白色沉淀 |
B. |
可以用澄清石灰水鉴别SO2和CO2 |
C. |
硫粉在过量的纯氧中燃烧可以生成SO3 |
D. |
SO2能使KMnO4水溶液迅速褪色 |
|
NA为阿伏加德罗常数,下列叙述错误的是 | |
| [ ] | |
A. |
18 g H2O中含的质子数为10NA |
B. |
标准状况下,11.2 L SO3中所含分子数目为0.5NA |
C. |
46 g NO2和N2O4混合气体中含有原子总数为3NA |
D. |
132 g硫酸铵中含有氮原子数目为2NA |