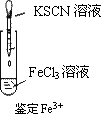
|
下列说法错误的是 | |
| [ ] | |
A. |
臭氧可使湿润的KI淀粉试纸变蓝 |
B. |
石英玻璃是以纯碱、石灰石和石英为原料制成的 |
C. |
用渗析法可分离淀粉胶体和碘化钾溶液的混合物 |
D. |
氯化亚铁溶液久置于空气中因被氧化而呈黄色 |
|
处理实验室有关事故方法不正确的是 | |
| [ ] | |
A. |
金属钠着火,立即浇水灭火 |
B. |
酒精灯碰翻着火,立即用湿抹布扑灭 |
C. |
汞滴洒落在地面上,立即撒上一层硫粉 |
D. |
皮肤沾上浓H2SO4,先用棉布吸去酸液,后立即用大量水冲洗 |
|
把物质的量均为0.1 mol的AlCl3、CuCl2和H2SO4溶于水制成100 ml的混合溶液,用石墨做电极电解,并收集两电极所产生的气体,一段时间后在两极收集到的气体在相同条件下体积相同.则下列描述正确的是 | |
| [ ] | |
A. |
电路中共转移0.9 mol电子 |
B. |
阳极得到的气体中有O2且其物质的量为0.35 mol |
C. |
阴极质量增加3.2 g |
D. |
铝元素以Al(OH)3的形式存在 |
|
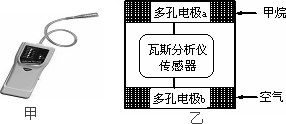
瓦斯爆炸是煤矿开采中的重大危害,一种瓦斯 分析仪(下图甲)能够在煤矿巷道中的甲烷浓度达到一定浓度时,可以通过传感器显示.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动.
下列有关叙述正确的的是 | |
| [ ] | |
A. |
瓦斯 分析仪工作时,电池内电路中电子由电极b流向电极a |
B. |
电极 b是正极,O2-由电极a流向电极b |
C. |
电极a 的反应式为:CH4+5O2――8e-=CO32-+2H2O |
D. |
当固体电解质中有 1 mol O2-通过时,电子转移4 mol |
|
一定条件下,碘单质与砹单质以等物质的量进行反应生成AtI.已知它与Zn、NH3都能发生反应,化学方程式分别如下: 2AtI+2Zn 下列关于AtI性质的叙述正确的是 | |
| [ ] | |
A. |
ZnI2既是氧化产物,又是还原产物 |
B. |
ZnAt2既是氧化产物,又是还原产物 |
C. |
AtI与液氨反应,AtI既是氧化剂,又是还原剂 |
D. |
AtNH2是一种强氧化性物质 |
|
F2和Xe在一定条件下可生成氧化性极强且极易水解的XeF2、XeF4和XeF6三种化合物.如XeF4 与水可发生如下反应:6XeF4+12H2O | |
| [ ] | |
A. |
F一般无正价,但在HFO中的F价态为+1 |
B. |
XeF2 分子中各原子均达到8电子结构 |
C. |
XeF4 按已知方式水解,反应中氧化剂为XeF4、还原剂为H2O |
D. |
XeF4 按已知方式水解,每生成4 mol Xe,转移16 mol电子 |
|
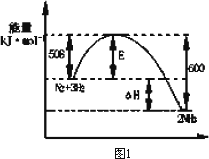
合成氨反应为:N2(g)+3H2(g)
下列说法正确的是: | |
| [ ] | |
A. |
该反应为自发反应,由图1可得加入适当的催化剂,E和ΔH都减小 |
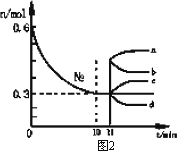
B. |
图2中0~10 min内该反应的平均速率v(H2)=0.045 mol·L-1·min-1,从11 min起其 它条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为d |
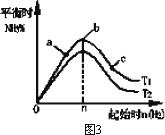
C. |
图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 |
D. |
图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是 | |
| [ ] | |
A. |
1 mol NO2与足量H2O反应,转移电子数为2 mol |
B. |
1 mol C5H12分子中含有的共价键数目为16NA |
C. |
1 L 0.5 mol/L Na2CO3溶液中阴离子数目小于0.5 mol |
D. |
CO2通过Na2O2使其增重b g时,反应中转移的电子数为 |
|
下列事实与氢键有关的是 | |
| [ ] | |
A. |
水加热到很高的温度都难以分解 |
B. |
NH3分子极易溶于水 |
C. |
CH4、SiH4、GeH4、SnH4的熔点随相对分子质量增大而升高 |
D. |
HF、HCl、HBr、HI的热稳定性依次减弱 |