|
将 40 mL 1.5 mol·L-1的CuSO4溶液与30 mL 3 mol·L-1的NaOH溶液混合生成浅蓝色沉淀,假如溶液中Cu2+或OH-浓度都已变得很小,可忽略,则生成沉淀的组成可表示为 | |
| [ ] | |
A. |
Cu(OH)2 |
B. |
CuSO4·Cu(OH)2 |
C. |
CuSO4·2Cu(OH)2 |
D. |
CuSO4·3Cu(OH)2 |
|
在t℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρg·cm-1,质量分数为ω,其中含NH4+的物质的量为b moL.下列叙述中正确的是 | |
| [ ] | |
A. |
溶质的质量分数为ω= |
B. |
溶质的物质的量浓度c= |
C. |
溶液中c(OH-)= |
D. |
上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω |
|
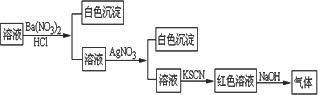
某同学为检验溶液中是否含有常见的四种无机离子,进行了下图所示的实验操作.其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝.由该实验能得到的正确结论是
| |
| [ ] | |
A. |
原溶液中一定含有 SO42-离子 |
B. |
原溶液中一定含有 NH4+离子 |
C. |
原溶液中一定含有 Cl-离子 |
D. |
原溶液中一定含有 Fe3+离子 |
|
将35 g锌粉与少量浓硫酸在加热条件下充分反应,共收集到混合气体11.2 L(标准状况),其质量为19.6 g,则过剩的锌粉的质量为 | |
| [ ] | |
A. |
1.0 g |
B. |
2.0 g |
C. |
2.5 g |
D. |
3.5 g |
|
通常状况下,NCl3是一种油状液体,其分子空间构型与氨分子相似,下列对NCl3的有关叙述正确的是 | |
| [ ] | |
A. |
CCl4中C-Cl键键长比NCl3中N-Cl键键长短 |
B. |
NCl3分子中四个原子共平面 |
C. |
分子中的所有原子均达到8电子稳定结构 |
D. |
NBr3比NCl3易挥发 |
|
为确定下列置于空气中的物质是否变质,所选检验试剂(括号内物质)不能达到目的的是 | |
| [ ] | |
A. |
Na2SO3溶液(BaCl2) |
B. |
FeCl2溶液(KSCN) |
C. |
KI(淀粉溶液) |
D. |
NaOH溶液(盐酸) |
|
下列实验操作或记录正确的是 | |
| [ ] | |
A. |
常温常压下测得1 mol N2的质量为28 g |
B. |
用量筒测得排水法收集制得的氢气体积为50.28 mL |
C. |
用两个250 mL的容量瓶配制0.1 mol/L 500 mL的NaOH溶液 |
D. |
用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
|
下列说法不正确的是 | |
| [ ] | |
A. |
区别溶液和胶体的方法是当一束光线通过胶体时可出现一条光亮的通路,溶液则没有此现象 |
B. |
将饱和FeCl3溶液滴入沸水中,继续加热煮沸至红褐色停止加热即得Fe(OH)3胶体 |
C. |
胶体带电荷,溶液不带电荷 |
D. |
土壤胶粒的比表面积巨大且一般带负电,能吸附NH |