|
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol/L Ba(OH)2溶液300 mL,反应后溶液中SO | |
| [ ] | |
A. |
0.4 mol/L |
B. |
0.3 mol/L |
C. |
0.2 mol/L |
D. |
0.1 mol/L |
|
浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合时,其溶质的质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是 | |
| [ ] | |
A. |
a>b>c |
B. |
b>a>c |
C. |
c>b>a |
D. |
c>a>b |
|
下列叙述正确的是 | |
| [ ] | |
A. |
同温同压下,相同体积的物质,它们的物质的量必相等 |
B. |
任何条件下,等物质的量的乙烯和一氧化碳所含的分子数必相等 |
C. |
1 L一氧化碳气体的质量一定比1 L氧气的质量小 |
D. |
等体积、等物质的量浓度的强酸中所含的H+数目一定相等 |
|
下列有关化学反应原理的应用叙述正确的是 | |
| [ ] | |
A. |
用明矾净水是因为Al3+水解生成的Al(OH)3胶粒具有很强的吸附性 |
B. |
合成氨生成过程中,采用高温高压都是为了提高N2、H2转化率 |
C. |
往铁钉镀铜时,用铜做阴极 |
D. |
电解饱和食盐水制烧碱,NaOH在阳极区域产生 |
|
在可逆反应2SO2+O2 | |
| [ ] | |
A. |
平衡右移,K变大,O2转化率增大 |
B. |
平衡右移,K变大,O2转化率减小 |
C. |
平衡右移,K不变,O2转化率增大 |
D. |
平衡右移,K不变,SO2转化率增大 |
|
t℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下该反应的平衡常数表达式为: | |
| [ ] | |
A. |
升高温度,平衡常数K一定增大 |
B. |
增大压强,W(g)质量分数增加 |
C. |
该反应的化学反应方程式为X+2Y |
D. |
增大X(g)浓度,平衡向逆反应方向移动 |
|
以惰性电极电解CuSO4和FeSO4溶液,若在阳极上产生气体的的体积在标准状况下为2.24 L,则阴极上析出的固体的质量为 | |
| [ ] | |
A. |
6.4 g |
B. |
12.8 g |
C. |
25.6 g |
D. |
5.12 g |
|
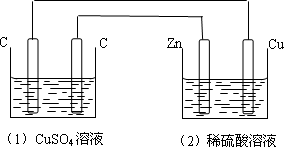
如图装置中,溶液体积均为200 ml,开始时,电解质溶液的浓度均为0.1 mol·L-1,工作一段时间后,测得导线上通过了0.02 mol电子,若不考虑溶液体积的变化,下列叙述中正确的是
| |
| [ ] | |
A. |
(1)、(2)两装置均为电解池 |
B. |
(1)、(2)溶液的PH均减小 |
C. |
(1)中阳极电极反应式为: 4OH--4e- 2H2O+O2↑ 2H2O+O2↑
|
D. |
(1)中阴极上析出0.32 g Cu |
 2SO3的平衡状态,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数)
2SO3的平衡状态,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数) xC(g)有如下图所示的关系曲线,下列说法正确的是
xC(g)有如下图所示的关系曲线,下列说法正确的是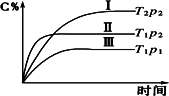
 2Z+2W
2Z+2W