|
甲试管中盛有 0.5 mol/L Na2CO3溶液10 mL,慢慢往试管中加入1 mol/L的盐酸7.0 mL;乙试管中盛有1 mol/L的盐酸7.0 mL,慢慢往试管中滴加0.5 mol/L Na2CO3溶液10 mL,那么甲、乙两试管中产生的CO2物质的量大小关系为 | |
| [ ] | |
A. |
甲=乙 |
B. |
甲>乙 |
C. |
甲<乙 |
D. |
无法确定 |
|
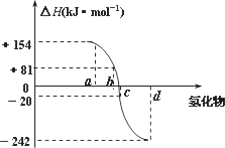
氧族元素包括氧、硫、硒、碲、钋等,下图为氧族元素氢化物a、b、c、d的生成热数据示意图,下列关于氧族元素的说明正确的
| |
| [ ] | |
A. |
含有18e-的两种氢化物中只存在极性键 |
B. |
氢化物的沸点大小是H2O<H2S<H2Se<H2Te |
C. |
a所对应的氢化物是H2O |
D. |
每1 mol H2S分解会吸收20 KJ的热 |
|
从下列事实所列出的相应结论合理的是 | |
| [ ] | |
A. |
SO2的水溶液可以导电说明是SO2电解质 |
B. |
常温下白磷可自燃而氮气须在放电时才与氧气反应说明N的非金属性大于P |
C. |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,该溶液一定有NH4+ |
D. |
某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-或HCO3- |
|
下列物质中所含指定的微粒数为阿伏加德罗常数的是 | |
| [ ] | |
A. |
常温常压下,2.2 g 14CD4所含质子数 |
B. |
常温常压下,46 g二氧化氮和四氧化二氮混合气体中所含氧原子总数 |
C. |
标准状况下,11.2 L H2O含有氢氧键 |
D. |
1.0 L 1 mol/L氨水中,NH3·H2O的分子数 |
|
在地壳内,深度每增加1 km,压强约增加25250~30300 kPa,这对固体物质的平衡会发生较大的影响.如 :CaAl2Si2O8+Mg2SiO4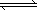 CaMg2Al2Si3O12 CaMg2Al2Si3O12
(钙长石) (镁橄榄石) (钙镁)石榴子石 密度(g/cm3) 2.70 3.22 3.50 则在地壳区域高压条件下,有利于 | |
| [ ] | |
A. |
钙长石生成 |
B. |
镁橄榄石生成 |
C. |
钙长石和镁橄榄石共存 |
D. |
(钙镁)石榴子石生成 |
|
向等体积等物质的量浓度的H2S和SO2的水溶液各两份中,分别通入Cl2和O2一段时间.下图表示通入的气体的量与溶液PH关系的曲线图,下列说法中正确的是:
| |
| [ ] | |
A. |
曲线b表示向H2S水溶液中通入O2 |
B. |
曲线b表示向SO2水溶液中通入O2 |
C. |
曲线c表示向H2S水溶液中通入Cl2 |
D. |
曲线d表示向SO2水溶液中通入Cl2 |
|
将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是 | |
| [ ] | |
A. |
1∶3 |
B. |
2∶5 |
C. |
1∶4 |
D. |
2∶7 |
|
密度为1.45 g/cm3的硫酸溶液中,逐滴加入BaCl2溶液,直到沉淀完全为止,已知沉淀的质量与原硫酸溶液相等,则原硫酸溶液的浓度为 | |
| [ ] | |
A. |
29.6% |
B. |
42.1% |
C. |
14.8 mol/L |
D. |
8 mol/L |
|
氨(NH3)是一种无色、极易溶于水的气体.在实验室加热氯化铵和熟石灰两种固体的混合物可制取氨气,则该实验可选用的制取装置和集气方法正确的是 | |
| [ ] | |
A. |
用启普发生器制取,用排水法收集 |
B. |
用启普发生器制取,用向下排空气法收集 |
C. |
与加热分解KClO3制氧气的装置相同,用向下排空气法收集 |
D. |
与加热分解KClO3制氧气的装置相同,用向上排空气法收集 |