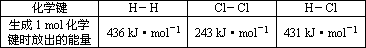|
下列与实验相关的叙述正确的是 | |
| [ ] | |
A. |
用托盘天平称量固体,固体不能直接放置在托盘中,都应该放在纸片上称量 |
B. |
分液时,下层液体先从下口放出,换一个接受容器,上层液体也从下口放出 |
C. |
浓硫酸不小心沾到皮肤上,可先用布擦,再用大量水冲洗,最后涂少量小苏打溶液 |
D. |
用pH试纸测未知溶液的pH时,若先润湿试纸再测量,则pH偏小 |
|
下列叙述不正确的是 | |
| [ ] | |
A. |
Al3+跟S2-在水溶液中发生比较彻底的双水解,所以用单质化合的方法制备Al2S3 |
B. |
用铝热反应原理可制得熔点较高的金属铁 |
C. |
电解MgCl2饱和溶液,可制得金属镁 |
D. |
在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
|
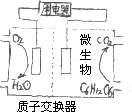
以葡萄糖为燃料的微生物燃料电池结构示意图如图所示,关于该电池的叙述正确的是
| |
| [ ] | |
A. |
该电池能够在高温下工作 |
B. |
电池的负极反应为:C6H12O6+6H2O-24e- |
C. |
放电过程中:H+从正极区向负极区迁移 |
D. |
在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体22.4/6 L |
|
在某100 mL混合酸中,HNO3物质的量浓度为0.4 mol/L,H2SO4物质的量浓度为0.2 mol/L.向其中加入1.92克铜粉微热,待充分反应后,溶液中的Cu2+物质的量浓度为 | |
| [ ] | |
A. |
0.15 mol/L |
B. |
0.3 mol/L |
C. |
0.225 mol/L |
D. |
无法计算 |
|
下列关于元素的叙述正确的是 | |
| [ ] | |
A. |
氟元素的非金属性最强,所以氢氟酸的酸性最强 |
B. |
元素的金属性越强,其最外层电子数就越少 |
C. |
一般元素简单阴离子的核外电子层数等于该元素所在的周期序数 |
D. |
Na2O、BaSO4、HCl、SO2在熔融状态下或溶于水时都能导电,所以都是电解质 |
|
在下列各溶液中,离子一定能大量共存的是 | |
| [ ] | |
A. |
强碱性溶液中:K+、Al3+、Cl-、SO42- |
B. |
含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
C. |
含有0.1 mol·L-1 Ca2+的溶液中:Na+、K+、CO32-、Cl- |
D. |
室温下,PH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
|
用NA表示阿伏加德罗常数的值,下列叙述正确的是 | |
| [ ] | |
A. |
25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
B. |
标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1NA |
C. |
1 L 1 mol/L的醋酸溶液中离子总数为2NA |
D. |
1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
|
日本地震导致核电站泄露出大量的人工放射性核素,如131I(碘)、137Cs(铯)等.下列说法正确的是 | |
| [ ] | |
A. |
放射性废水的处理方法主要有稀释排放法、放置衰变法、沥青固化法等. |
B. |
127 I是碘元素稳定的同位素,与131I为互为同分异构体 |
C. |
127 I与131I的质量数不同,核外电子排布方式也不同 |
D. |
铯为IA元素,常温时,0.1 mol·L-1的137CsOH溶液,pH<13 |
|
反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应: (1)2NaI+MnO2+3H2SO4 (2)2NaIO3+5NaHSO3 下列说法正确的是 | |
| [ ] | |
A. |
两个反应中NaHSO4均为氧化产物 |
B. |
I2在反应(1)是还原产物,在反应(2)中是氧化产物 |
C. |
氧化性:MnO2>SO |
D. |
反应(1)、(2)中生成等量的I2时转移电子数比为1∶5 |
|
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
则下列热化学方程式不正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
H2(g)+Cl2(g)=2HCl(g);ΔH=-183 kJ·mol-1 |
D. |
2HCl(g)=H2(g)+Cl2(g);ΔH=+183 kJ·mol-1 |
 6CO2↑+24H+
6CO2↑+24H+ 2NaHSO4+MnSO4+2H2O+I2
2NaHSO4+MnSO4+2H2O+I2 2Na2SO4+3NaHSO4+H2O+I2
2Na2SO4+3NaHSO4+H2O+I2