|
设 NA为阿伏加德罗常数,下列说法正确的是 | |
| [ ] | |
A. |
23 g Na在氧气中完全燃烧失电子数为0.5NA |
B. |
1 L 2 mol·L-1的MgCl2溶液中含Mg2+数为2NA |
C. |
标准状况下, 11.2 L SO3所含分子数为0.5NA |
D. |
室温下, 8 g甲烷含有共价键数为2NA |
|
氯气是一种重要的工业原料.工业上利用反应在 3Cl2+2NH3 N2+6HCl,检查氯气管道是否漏气.下列说法错误的是 N2+6HCl,检查氯气管道是否漏气.下列说法错误的是
| |
| [ ] | |
A. |
若管道漏气遇氨就会产生白烟; |
B. |
该反应利用了 Cl2的强氧化性 |
C. |
该反应属于复分解反应; |
D. |
生成 1 mol N2有6 mol电子转移 |
|
H2、N2、O2三种气体分别放入不同容器中,使它们的温度、密度相同,则其压强(P)大小的关系,符合的是 | |
| [ ] | |
A. |
P(H2)>P(O2)>P(N2) |
B. |
P(O2)>P(N2)>P(H2) |
C. |
P(H2)>P(N2)>P(O2) |
D. |
P(N2)>P(O2)>P(H2) |
|
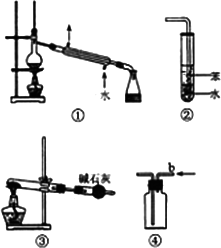
关于下列各实验装置图的叙述中,正确的是
| |
| [ ] | |
A. |
装置①可用于分离苯和溴苯的混合物 |
B. |
装置②可用于吸收HC1或NH3气体 |
C. |
装置③可用于分解NH4C1制备NH3 |
D. |
装置④b口进气可收集CO2或NO气体 |
|
已知氯化铁溶液中通入硫化氢可发生反应:2FeCl3+H2S→2FeCl2+S↓+2HCl.在标准状况下,向100 mL FeCl3溶液中通入aL的H2S气体恰好反应后,再加入足量的铁粉充分反应.所得溶液经测定金属阳离子的浓度为3 mol/L,若反应过程中溶液体积不变,则原FeCl3溶液的物质的量浓度为 | |
| [ ] | |
A. |
1.5 mol/L |
B. |
2 moi/L |
C. |
l mol/L |
D. |
无法确定 |
|
下列实验目的可以达到的是 | |
| [ ] | |
A. |
醋酸钠结晶水合物与碱石灰共热制取甲烷 |
B. |
配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
C. |
一般仅用蒸馏水就能鉴别出食盐、烧碱、硝酸铵三种固体 |
D. |
用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液 |
|
下列排列顺序正确的是 ①热稳定性:H2O>HF>H2S ②原子半径:Na>Mg>O ③酸性:H3PO4>H2SO4>HClO4 ④离子半径:O2->F->Na+ | |
| [ ] | |
A. |
①③ |
B. |
②④ |
C. |
①④ |
D. |
②③ |
|
下图为实验室制氢气的简易装置.若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸不够了,为使该反应顺利进行,可以从长颈漏斗中加入的试剂是 ①食盐水 ②KNO3溶液 ③适量稀硫酸铜溶液 ④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
| |
| [ ] | |
A. |
①③⑤ |
B. |
①②③ |
C. |
④⑤⑥ |
D. |
①②③⑤ |