|
在硫酸的工业生产中,下列生产操作及对生产操作主要原因的说明二者都正确的是 | |
| [ ] | |
A. |
从沸腾炉出来的炉气需净化,因为炉气中SO2会与杂质反应 |
B. |
硫铁矿燃烧前需要粉碎,因为大块的不能燃烧 |
C. |
SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,以使SO3吸收完全 |
D. |
SO2氧化为SO3时需使用催化剂,这样可以提高SO2的转化率 |
|
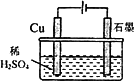
某同学按图所示的装置进行电解实验.下列说法正确的是
| |
| [ ] | |
A. |
电解过程中,铜电极上有H2产生 |
B. |
电解初期,主反应方程式为:Cu+H2SO4 |
C. |
电解一段时间后,石墨电极上有O2产生 |
D. |
整个电解过程中,H+的浓度不断增大 |
|
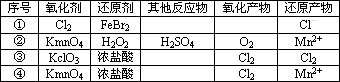
根据下表信息,下列叙述中正确的是
| |
| [ ] | |
A. |
第①组反应中的氧化产物一定只有FeCl3 |
B. |
氧化性强弱比较:KMnO4>O2>Fe3+>Cl2>Fe2+ |
C. |
还原性强弱比较:H2O2>Mn2+>Cl- |
D. |
④的离子方程式配平后,H+的化学计量数为16 |
|
已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H-O键形成时放出热量463 kJ,则氢气中1 mol H-H键断裂时吸收热量为 | |
| [ ] | |
A. |
920 kJ |
B. |
557 kJ |
C. |
436 kJ |
D. |
188 kJ |
|
有Fe2+、 | |
| [ ] | |
A. |
氧化剂与还原剂的物质的量之比为8∶1 |
B. |
还原产物为 |
C. |
若有1 mol |
D. |
若把该反应设计原电池,则负极反应为:Fe2+-e-=Fe3+ |
|
体育比赛中使用的发令枪中所用的“火药”成分是氯酸钾和红磷,经撞击发出响声,同时产生白色烟雾.撞击时发生的化学反应方程式为:5KClO3+6P=3P2O5+5KCl,则下列有关叙述错误的是 | |
| [ ] | |
A. |
上述反应中氧化剂和还原剂的物质的量之比为5∶6 |
B. |
产生白色烟雾的原因是生成的P2O5白色固体小颗粒(烟)吸水性很强,吸收空气中的水分,生成酸滴(雾) |
C. |
上述反应中消耗3 mol P时,转移电子的物质的量为15 mol |
D. |
因红磷和白磷互为同分异构体,所以上述火药中的红磷可以用白磷代替 |
|
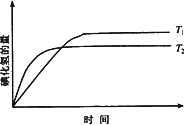
在密闭窗口中进行如下反应:H2(g)+I2(g)
| |
| [ ] | |
A. |
T1>T2,ΔH>0 |
B. |
T1>T2,ΔH<0 |
C. |
T1<T2,ΔH>0 |
D. |
T1<T2,ΔH<0 |
|
下列现象或应用不能用胶体知识解释的是 | |
| [ ] | |
A. |
肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
B. |
牛油与NaOH溶液共煮,向反应后所得的溶液中加入食盐析出固体 |
C. |
氯化铝溶液中加入小苏打溶液会产生白色沉淀和气体 |
D. |
水泥冶金厂常用高压电除去工厂烟尘,减少对空气污染 |
 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如下图所示.符合图示的正确判断是