|
将一定体积稀硝酸溶液平均分为两份,一份与足量的铜粉反应收集到气体体积为V1;另一份先加入与其等体积的稀硫酸,再投入足量的铜粉收集到气体的体积为V2(V1和V2都在同一条件下测定),已知V2=3V1,则稀硝酸和稀硫酸的物质的量浓度之比 | |
| [ ] | |
A. |
1∶1 |
B. |
10∶2 |
C. |
100∶3 |
D. |
无法确定 |
|
石墨能与熔融金属钾作用 ,形成石墨间隙化合物,K原子填充在石墨各层碳原子中,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,其平面结构见下图,则x值为
| |
| [ ] | |
A. |
8 |
B. |
12 |
C. |
24 |
D. |
60 |
|
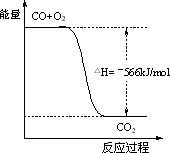
已知 :2CO(g)+O2(g)=2CO2(g);ΔH=-566 kJ/molNa2O2(s)+CO2(g)=Na2CO3(s)+1/2O2(g); ΔH=-226 kJ/mol根据以上热化学方程式判断,下列说法正确的是
| |
| [ ] | |
A. |
CO的燃烧热为283 kJ |
B. |
上图可表示由CO生成CO2的反应过程和能量关系 |
C. |
2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g); ΔH>-452 kJ/mol |
D. |
CO(g) 与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
|
下列说法正确的是 | |
| [ ] | |
A. |
仅用AgNO3溶液便可鉴别纯碱和食盐 |
B. |
重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 |
C. |
乙酸与乙醇的混合液可用分液漏斗进行分离 |
D. |
用盐酸标准溶液滴定待测氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
|
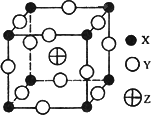
已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,X、Y、Z分别处于立方体的顶点、棱边的中点、立方体的体心.则下面表示该化合物的化学式正确的
| |
| [ ] | |
A. |
ZXY3 |
B. |
ZX2Y6 |
C. |
ZX4Y8 |
D. |
ZX8Y12 |
|
下列有关实验操作的说法正确的是 | |
| [ ] | |
A. |
可用25 mL碱式滴定管量取20.00 mL KMnO4溶液 |
B. |
用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 |
C. |
蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干 |
D. |
将金属钠在研体中研成粉末,使钠与水反应的实验更安全 |
|
在相同状况下,下列两个反应放出的热量分别用Q1、Q2表示:H2(g)+1/2O2(g)═H2O(g),2H2(g)+O2(g)═2H2O(l),则Q1和Q2的关系正确的是 | |
| [ ] | |
A. |
Q1>Q2 |
B. |
Q1=Q2 |
C. |
Q1<Q2 |
D. |
Q1=1/2Q2 |
|
下列推断合理的是 | |
| [ ] | |
A. |
明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
B. |
金刚石是自然界中硬度最大的物质,不可能与氧气发生反应 |
C. |
浓H2SO4有强氧化性,常温下能与Cu发生剧烈反应 |
D. |
将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色 |
|
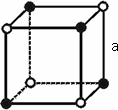
已知NaCl的摩尔质量为58.5 g·mol-1,其晶体密度为d g·cm-3,若下图中钠离子与最接近的氯离子的核间距离为a cm,那么阿伏加德罗常数的值可表示
| |
| [ ] | |
A. |
117a3d |
B. |
58.5/(2a3d) |
C. |
234/(a3d) |
D. |
58.5/(4a3d) |