|
下列图示与对应的叙述相符的是 | |
| [ ] | |
A. |
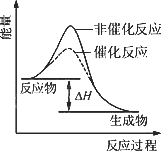
下图表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化
|
B. |
下图表示0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得到的滴定曲线 |
C. |
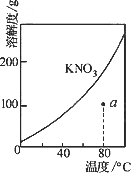
下图表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
|
D. |
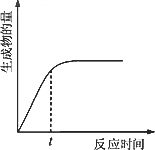
下图表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大
|
|
下列有关实验原理或实验操作正确的是 | |
| [ ] | |
A. |
用水湿润pH试纸测量某溶液的pH |
B. |
用量筒量取20 mol·L-1 H2SO4溶液于烧杯中,加水80 mL,配制成0.1000 mol·L-1 H2SO4溶液 |
C. |
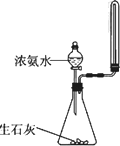
实验室用下图所示装置制取少量氨气
|
D. |
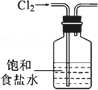
实验室用下图所示装置出去Cl2中的少量HCl
|
|
下列有关物质的性质和该性质的应用均正确的是 | |
| [ ] | |
A. |
常温下浓硫酸能是铝发生钝化,可在常温下作用铝制贮藏贮运浓硫酸 |
B. |
二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
C. |
二氧化氯具有还原性,可用于自来水的杀菌消毒 |
D. |
铜的金属活泼性比铁的若,可在海轮外壳上装若干铜块以减缓其腐蚀 |
|
用石墨作电极电解1 mol/L CuSO4溶液,当c(Cu2+)为0.5 mol/L时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来状况 | |
| [ ] | |
A. |
CuSO4 |
B. |
CuO |
C. |
Cu(OH)2 |
D. |
CuSO4·5H2O |
|
三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调节NiCl2溶液pH至7.5,加入适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.以下说法正确的是 | |
| [ ] | |
A. |
可用铁作阳极材料 |
B. |
电解过程中阳极附近溶液的pH升高 |
C. |
阳极反应方程式为:2Cl--2e- |
D. |
1 mol二价镍全部转化为三价镍时,外电路中通过了2 mol电子 |
|
按如图所示的装置进行电解实验:A极是铜锌合金,B极为纯铜,电解质溶液为硫酸铜溶液(足量).通电一段时间后,A极恰好全部溶解,此时B极质量增加7.68 g,溶液质量增加0.03 g,则A合金中铜、锌原子个数比为
| |
| [ ] | |
A. |
4∶1 |
B. |
3∶1 |
C. |
2∶1 |
D. |
任意比 |
|
下列关于铜电极的叙述正确的是 | |
| [ ] | |
A. |
铜锌原电池中铜电极上发生氧化反应 |
B. |
电解饱和食盐水制烧碱时,用铜作阳极 |
C. |
电解法精炼铜时,粗铜连接电源的正极 |
D. |
电镀铜和精炼铜时,均用纯铜作阴极 |
|
近年,科学家们发明了一种能够给电子设备提供动力的生物燃料电池.该电池包括两个涂覆着酶的电极,它们处于充满空气和少量氢气的玻璃槽中.由于气体可以混合从而省去了昂贵的燃料隔离膜,其工作原理如图所示.下列说法正确的是
| |
| [ ] | |
A. |
左边为该电池的负极 |
B. |
该电池可在高温环境下使用 |
C. |
该电池负极反应为:H2-2e- |
D. |
该电池正极反应为O2+4e- |
 Cl2↑
Cl2↑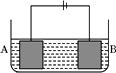

 2H+
2H+ 2O2-
2O2-