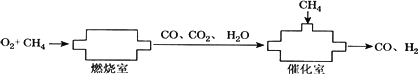|
CO和H2是有机合成的重要原料.某化学小组拟用下列装置抽取合成气CO、H2O.将x mol O2和一定量CH4在燃烧室中不完全燃烧,产生的物质完全进入催化室与CH4恰好完全反应,生成CO和H2.则从催化室中出来的H2为
| |
| [ ] | |
A. |
x mol |
B. |
3x mol |
C. |
4x mol |
D. |
5x mol |
|
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB=2VC,且VA=VB+VC,则在A的生成物中,该金属元素的化合价为 | |
| [ ] | |
A. |
+1 |
B. |
+2 |
C. |
+3 |
D. |
+4 |
|
a mL浓度为c mol/L的AgNO3溶液中加入一定体积的pH=1的盐酸时,恰好使溶液中的Ag+完全沉淀,此时得到pH=2的溶液100 mL(设反应前后溶液体积变化忽略不计),则c的值是 | |
| [ ] | |
A. |
0.0020 |
B. |
0.011 |
C. |
0.11 |
D. |
0.22 |
|
一定温度和压强下,8 g A和17 g B的混合气体的体积为900 mL,相同状况下,4 g A和14 g B的混合气体的体积为600 mL.则A和B可能分别是下列各组中的 | |
| [ ] | |
A. |
CH4和O2 |
B. |
CO和CO2 |
C. |
NH3和NO |
D. |
H2和CH4 |
|
下列叙述一定正确的是 | |
| [ ] | |
A. |
室温下,将pH=a的醋酸溶液稀释10倍,溶液的pH=b,则b=a+1 |
B. |
在滴有酚酞溶液的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
C. |
90℃下,1.0×10-3 mol/L盐酸的pH=3.0,1.0×10-6 mol/L烧碱溶液的pH=8.0 |
D. |
室温下,若1 mL pH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7,则混合前NaOH溶液的pH=11 |
|
按规定在食盐中添加一定量的碘化钾(KIO3)即成为可以为人体补充碘元素的“加碘食盐”.KIO3可用在一定温度下电解KI水溶液的方法制得.以下关于这一生产得叙述正确的是 | |
| [ ] | |
A. |
KIO3 在阳极产生,阴极产物为H2 |
B. |
可以用不锈钢棒作两个电极的材料 |
C. |
产生IO |
D. |
溶液中阳离子向阳极移动 |
|
下列有关原电池和电解池的叙述中正确的是 | |
| [ ] | |
A. |
钢管大部分浸在淡水中,主要发生析氢腐蚀 |
B. |
钢管若采用外加电流的阴极保护措施,应当与电源的正极相连 |
C. |
钢管若需保护,可采用牺牲阳极的阴极保护法 |
D. |
电解氯化钠溶液时电子从负极经过溶液流向正极 |
|
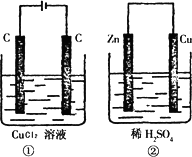
如图所示的两个实验装置中,溶液的体积均为200 mL,开始时电解质溶液的浓度均为0.1 mol/L,工作一段时间后,测得导线中均通过0.02 mol电子,若不考虑气体的溶解和溶液体积的变化,则下列叙述中正确的是
| |
| [ ] | |
A. |
产生气体的体积:①>② |
B. |
电极上析出物质的质量:①>② |
C. |
溶液的pH变化:①增大,②减小 |
D. |
电极反应式:②中负极:Zn ―2e― |