|
常温下,下列各组粒子在指定溶液中能大量共存的是 | |
| [ ] | |
A. |
pH=l的溶液中:CH3CH2OH、Cr2O |
B. |
NaHCO3溶液中: |
C. |
加入铝粉放出大量H2的溶液中:Fe2+、K+、Cl-、NO |
D. |
C(Ca2+)=0.1 mol·L-1的溶液中:NH |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是 | |
| [ ] | |
A. |
含有NA个NO2、N2O4分子的混合气体降低温度,混合气体的分子数目小于NA |
B. |
常温常压和光照条件下,33.6 L Cl2与3.0 g H2反应,生成的HCl分子数目为3 NA |
C. |
1.68 g Fe和足量水蒸气反应,转移的电子数目为0.09 NA |
D. |
一定条件下,1 mol N2和3 mol H2充分反应,生成物中含N-H键数目为6 NA |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
用FeCl3溶液腐蚀铜线路板:Cu+Fe3+=Cu2++Fe2+ |
B. |
用稀硝酸清洗做过银镜反应的试管:Ag+NO |
C. |
向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
D. |
用二氧化锰与浓盐酸反应制取Cl2:MnO2+4H++2Cl- |
|
科学家合成了一系列独特的氢铝化合物.最简单的氢铝化合物化学式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如下图.下列有关说法不正确的是
| |
| [ ] | |
A. |
Al2H6中Al为-3价,H为+1价 |
B. |
Al2H6在空气中完全燃烧,产物为氧化铝和水 |
C. |
Al2H6 是共价化合物 |
D. |
氢铝化合物可能成为未来的储氢材料和火箭燃料 |
|
镁钼蓄电池的总反应为:xMg+Mo3S4 | |
| [ ] | |
A. |
放电时电能转化为化学能 |
B. |
放电时负极的电极反应为:Mg-2e- |
C. |
充电时Mg2+向阳极移动 |
D. |
充电时Mo3S42x-发生还原反应 |
|
某条件下,恒容密闭容器中发生反应 :CO2(g)+3H2(g) | |
| [ ] | |
A. |
用高效 催化剂,可使CO2的平衡转化率增大 |
B. |
单位时间内消耗CO2和H 2的物质的量比为1∶3时,反应达到平衡 |
C. |
及时分离出CH3OH和 H2O可提高CO2和H2的转化率 |
D. |
升高温度可使该反应的平衡常数增大 |
|
第三周期元素X、Y、Z,其最高价氧化物的化学式分别为X2O、Y2O3、ZO2,下列有关判断错误的是 | |
| [ ] | |
A. |
原子半径X<Y<Z |
B. |
三种元素中X的金属性最强 |
C. |
Y(OH)3能与NaOH溶液反应 |
D. |
ZO2可制造光导纤维 |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
向明矾溶液加入过量氨水:Al3++4OH- |
B. |
碳酸钙溶于稀盐酸:CO |
C. |
铜与稀硝酸反应:3Cu+2NO |
D. |
一小块钠投入到CuSO4溶液中:2Na+Cu2+ |
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O CO
CO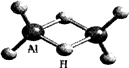
 MgxMo3S4;下列说法正确的是
MgxMo3S4;下列说法正确的是 Mg2+
Mg2+ CH3OH(g)+H2O(g);
CH3OH(g)+H2O(g);
 Al(OH)
Al(OH) H2O+CO2↑
H2O+CO2↑ 3Cu2++2NO↑+4H2O
3Cu2++2NO↑+4H2O Cu+2Na+
Cu+2Na+