|
化学用语是学习化学的重要工具.以下化学用语表示 错误的是 | |
| [ ] | |
A. |
质量数之和是质子数之和两倍的水分子符号可能是:D |
B. |
NaHCO3水溶液呈碱性的原因:HCO |
C. |
基态硫离子的电子排布式:1s22s22p63s23p6 |
D. |
熔融状态下硫酸氢钠的电离方程式:NaHSO4(熔融)=Na++HSO |
|
以下物质检验的结论可靠的是 | |
| [ ] | |
A. |
往溶液中加入浓溴水,出现白色沉淀,说明含有苯酚 |
B. |
往无色溶液中加入氯水,再加CCl4,CCl4层呈红棕色,说明有Br- |
C. |
在制备乙酸乙酯后剩余的反应液中加入碳酸钠溶液,产生气泡,说明还有乙酸剩余 |
D. |
将乙醇和浓硫酸共热后得到的气体通入溴水中,溴水褪色,说明生成了乙烯 |
|
用NA表示阿伏加德罗常数,下列叙述中正确的是 | |
| [ ] | |
A. |
22.4 L N2和NH3混合气体中原子间共有3 NA个共用电子对 |
B. |
3.0 g甲醛和乙酸混合物中共含碳原子数为0.1 NA |
C. |
25℃时pH=1的醋酸溶液中含有H+的数目为0.1 NA |
D. |
标准状况下,2.24 L CHCl3含有的分子数为0.1 NA |
|
下列描述,其因果关系成立的是 | |
| [ ] | |
A. |
因为NH3的水溶液可以导电,所以NH3是电解质 |
B. |
因为SO2可以使溴水褪色,所以SO2具有漂白性 |
C. |
因为某碱性溶液的焰色呈黄色,所以其溶质为NaOH |
D. |
因为电解质溶于水后电离为离子,所以电解质在溶液中的反应实质是离子反应 |
|
学习时通过比较、归纳,可以加深对问题的认识.下列比较或归纳一定正确的是 | |
| [ ] | |
A. |
稳定性:NH3<PH3<AsH3 |
B. |
离子半径:阴离子>阳离子 |
C. |
熔沸点:离子化合物>共价化合物 |
D. |
酸性:H2SO4>H3PO4>H2SiO3 |
|
已知相同温度下电离常数Ki(HF)>Ki(HCN).在物质的量浓度均为0.1 mol/L的NaCN和NaF混合溶液中,下列关系正确的是 | |
| [ ] | |
A. |
c(F-)>c(OH-)>c(HCN)>c(HF) |
B. |
c(F-)+c(HF)>c(CN-)+c(HCN) |
C. |
c(OH-)>c(F-)>c(CN-)>c(H+) |
D. |
c(OH-)>c(HF)>c(HCN)>c(H+) |
|
下列实验设计与结论相符合的是 | |
| [ ] | |
A. |
将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘单质萃取到乙醇中 |
B. |
某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液显碱性 |
C. |
某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定含有SO |
D. |
在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液 |
|
在下列给定条件的水溶液中,一定能大量共存的离子组是 | |
| [ ] | |
A. |
能 与铝反应生成H2的溶液:Ca2+、NH |
B. |
存在大量 Fe2+的溶液:H+、Na+、NO |
C. |
由水电离出的c(H+)=10-12 mol/L 的溶液:Na+、K+、Cl-、NO |
D. |
常温下,c(H+)∶c(OH-)=1×10-12的溶液:K+、Ba2+、ClO-、CO |
|
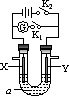
如图所示,X为铁、Y是石墨电极,a是饱和食盐水,实验开始前,在U形管的两边同时各滴入几滴酚酞试液,下列叙述错误的是
| |
| [ ] | |
A. |
合上K1、断开K2,该装置可以将化学能转变为电能 |
B. |
合上K1、断开K2,X是阴极,Y电极附近溶液慢慢变为红色 |
C. |
合上K2、断开K1,湿润的KI淀粉试纸靠近Y电极管口,试纸变蓝 |
D. |
合上K2、断开K1,电解一段时间,X电极附近溶液呈红色 |