|
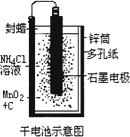
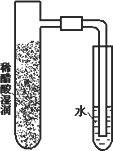
普通锌锰干电池的简图(如下图所示),它是用锌皮制成的锌筒作电极兼做容器,中央插一根碳棒,碳棒顶端加一铜帽.在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为: Zn+2NH4++2MnO2 关于锌锰干电池的下列说法中正确的是
| |
| [ ] | |
A. |
当该电池电压逐渐下降后,利用电解原理能重新充电复原 |
B. |
电池正极的电极反应式为: 2MnO2+2NH4++2e- |
C. |
电池工作时,电子由正极通过外电路流向负极 |
D. |
外电路中每通过0.1 mol电子,锌的质量理论上减小6.5 g |
|
镍氢电池是近年来开发出来的可充电电池,它可取代会产生镉污染的镍镉电池.镍氢电池的总反应式是H2+2NiO(OH) 根据此反应式判断,下列叙述正确的是 | |
| [ ] | |
A. |
电池放电时,某电极上电极反应为:Ni3++e-→Ni2+ |
B. |
电池放电时,Ni(OH)2的含量不断减少 |
C. |
电池充电时,镍元素被还原 |
D. |
电池放电时,H2是负极 |
|
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为: 3Zn+2K2FeO4+8H2O 下列叙述不正确的是 | |
| [ ] | |
A. |
放电时负极反应为:3Zn-6e-+6OH- |
B. |
放电时正极反应为:2FeO42-+6e-+8H2O |
C. |
放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
D. |
放电时正极附近溶液的碱性增强 |
|
燃烧1 g乙炔(C2H2)生成二氧化碳和液态水,放出热量50 kJ,则这一反应的热化学反应方程式为 | |
| [ ] | |
A. |
2C2H2(g)+5O2(g) |
B. |
C2H2(g)+5/2O2(g) |
C. |
2C2H2+5O2 |
D. |
2C2H2(g)+5O2(g) |
|
下列说法正确的是 | |
| [ ] | |
A. |
任何化学反应都伴随着能量的变化 |
B. |
1 mol H2SO4和1 mol Ba(OH)2完全反应所放出的热量称为中和热 |
C. |
在101 kPa时,1 mol碳燃烧放出的热量就是碳的燃烧热 |
D. |
在化学反应中需要加热的反应就是吸热反应 |
|
在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是 | |
| [ ] | |
A. |
XY3晶体一定是离子晶体 |
B. |
若Y的原子序数为m,X的原子序数一定是m±4 |
C. |
X和Y可属于同一周期,也可属于两个不同周期 |
D. |
X和Y一定不属于同一主族 |
|
科学界拟合成一种“双重结构”的球形分子,即把足球烯C60分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列有关叙述正确的是 | |
| [ ] | |
A. |
该反应属于置换反应 |
B. |
该物质是一种新型化合物 |
C. |
该物质具有极高的熔沸点 |
D. |
该晶体属于原子晶体 |
|
下图所示的结构图中,均为由短周期元素的原子构成的分子,●代表原子实(原子实是原子除去最外层电子后剩余部分),小黑点代表未用于形成共价键的最外层电子,一条短线代表一对共用电子对.下列图甲和图乙所表示的分子依次是
| |
| [ ] | |
A. |
HClO、AlCl3 |
B. |
NaOH、NH3 |
C. |
LiOH、PCl3 |
D. |
HCN、BF3 |
|
最新科技报导,美国夏威夷联合天文中心的科学家发现了新型氢微粒,这种新微粒是由3个氢原子核(只含质子)和2个电子构成,对于这种微粒,下列说法中正确的是 | |
| [ ] | |
A. |
是氢的一种新的同素异形体 |
B. |
是氢的一种新的同位素 |
C. |
它比一个普通H2分子多一个氢原子核 |
D. |
它的组成可用H3表示 |