|
关于某无色溶液中所含离子的鉴别 ,下列判断正确的是 | |
| [ ] | |
A. |
加入 AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在 |
B. |
加入 Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定SO42-存在 |
C. |
通入 Cl2后,溶液变为黄色,加入淀粉溶液后溶液变蓝,可确定有I-存在 |
D. |
加入盐酸,生成的气体能使澄清石灰水变浑浊,则原溶液中一定有大量CO32- |
|
下列溶液中氯离子的物 质的量浓度与50 mL 1 mol·L-1氯化铝溶液中氯离子的物质的量浓度相等的是 | |
| [ ] | |
A. |
150 mL 1 mol·L-1 氯化钠溶液 |
B. |
75 mL 2 mol·L-1 氯化铵溶液 |
C. |
150 mL 3 mol·L-1 氯化钾溶液 |
D. |
50 mL 3 mol·L-1 氯化亚铁溶液 |
|
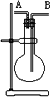
某学生想利用下图装置(烧瓶位置不能移动)收集下列气体:
①H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦NO2 ⑧SO2, 下列操作正确的是 | |
| [ ] | |
A. |
烧瓶是干燥的,由A进气收集①③⑤ |
B. |
烧瓶是干燥的,由B进气收集②④⑥⑦⑧ |
C. |
在烧瓶中充满水,由A进气收集①③⑤⑦ |
D. |
在烧瓶中充满水,由B进气收集⑥ |
|
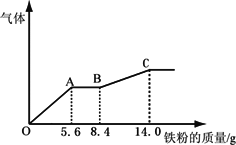
某稀硫酸和稀硝酸的混合溶液 200 mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6 g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体).下列分析或结果不正确的是
| |
| [ ] | |
A. |
原 混合酸中NO3-物质的量为0.2 mol |
B. |
原混合酸中H2SO4浓度为2 mol·L -1 |
C. |
OA 段产生的气体是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生的气体是氢气 |
D. |
第二份溶液中最终溶质为FeSO4 |
|
在不引入新杂质的情况下,分离FeCl3、KCl、BaSO4的混合物,应选用的一组试剂是 | |
| [ ] | |
A. |
水、AgNO3溶液、稀HNO3 |
B. |
水、NaOH溶液、稀HCl |
C. |
水、KOH溶液、稀HCl |
D. |
水、KOH溶液、稀HNO3 |
|
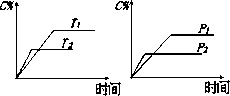
可逆反应aA(s)+bB(g)
下列叙述正确的是 | |
| [ ] | |
A. |
达平衡后,加入催化剂则C%增大 |
B. |
达平衡后,若升温,平衡左移 |
C. |
化学方程式中c+d>a+b |
D. |
达平衡后,增大压强有利于平衡向右移动 |
|
下列叙述正确的是 | |
| [ ] | |
A. |
加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42- |
B. |
滴入KMnO4酸性溶液,紫红色褪去,证明CH2=CHCH2CHO中一定有碳碳不饱和键 |
C. |
某无色气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 |
D. |
加入稀盐酸,产生无色并能使澄清石灰水变浑浊的气体,原溶液一定有CO32-或SO32- |