|
在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应: A(s)+2B(g) | |
| [ ] | |
A. |
混合气体的平均摩尔质量 |
B. |
混合气体的密度 |
C. |
A物质的质量 |
D. |
气体的总物质的量 |
|
已知H2(g)+Br2(l)=2HBr(g);ΔH=-72 kJ/mol.蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其它相关数据如下表:
则表中a为 | |
| [ ] | |
A. |
404 |
B. |
260 |
C. |
230 |
D. |
200 |
|
美国科学家成功开发便携式固体氧化物燃料电池,它以丙烷气体为燃料,每填充一次燃料,大约可连续24小时输出50 W的电力.一极通人空气,另一极通人丙烷气体,电解质是固态氧化物,在熔融状态下能传导O2-,下列对该燃料电池的说法不正确的是 | |
| [ ] | |
A. |
电路中每流过5 mol电子,肯定有5.6 L丙烷被完全氧化 |
B. |
该电池的总反应是:C3H8+5O2→3CO2+4H2O |
C. |
在熔融电解质中,O2-由正极移向负极 |
D. |
通丙烷的电极为电池负极,发生的电极反应为:C3H8-20e-+10O2- |
|
下列叙述正确的是 | |
| [ ] | |
A. |
电解法精炼铜时,电解质溶液中铜离子浓度一定不变 |
B. |
甲醇和氧气以及KOH溶液构成的新型燃料电池中,其正极上发生的反应为: CH3OH -6e-+8OH- |
C. |
在铁上镀铜时,金属铜作阴极 |
D. |
溶液、胶体和悬浊液三种分散系的本质区别是分散质微粒直径的大小 |
|
将 a g无水Na2CO3溶于t℃的饱和Na2CO3溶液中,析出b g晶体,则(b-a)g表示的含义是 | |
| [ ] | |
A. |
减少的饱和溶液的质量 |
B. |
饱和溶液失去溶质Na2CO3的质量 |
C. |
析出Na2CO3·10H2O的质量 |
D. |
饱和溶液失去水的质量 |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
过量的CO2通入Ca(ClO)2溶液中2ClO-+CO2+H2O |
B. |
AgNO3溶液滴入少量的Na2S溶液2Ag++S2-=Ag2S↓ |
C. |
向Na2CO3溶液中加入过量CH3COOH溶液CO32-+2H+ |
D. |
向Ba(OH)2溶液中加入少量的NaHSO3溶液 2HSO3-+Ba2++2OH- |
|
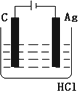
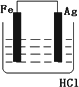
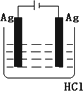
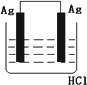
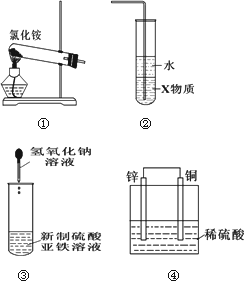
关于下列各装置图的叙述中 ,正确的是
| |
| [ ] | |
A. |
实验室用装置①制取氨气 |
B. |
装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
C. |
装置③可用于制备氢氧化亚铁并观察其颜色 |
D. |
装置④是原电池,锌电极为负极,发生还原反应 |
|
取少量无机盐溶液试样对其中的离子进行检验.下列判断正确的是 | |
| [ ] | |
A. |
加入盐酸,产生白色沉淀,则试样中一定有Ag+ |
B. |
加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32- |
C. |
加入BaCl2溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解,则试样中一定有SO42 |
D. |
加入NaOH溶液微热,产生能使湿润的红色石蕊试纸变蓝的气体,则试样中一定有NH4+ |
|
在含有FeCl3和BaCl2的酸性溶液中,通入足量的SO2后有白色沉淀生成,过滤后,向溶液中滴加KSCN溶液,无明显现象,下列叙述正确的是 | |
| [ ] | |
A. |
白色沉淀是BaSO4和BaSO3 |
B. |
溶液的酸性减弱 |
C. |
白色沉淀是BaSO3 |
D. |
FeCl3全部被还原为FeCl2 |