|
用NA表示阿伏加德罗常数的值.下列叙述正确的是 | |
| [ ] | |
A. |
室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
B. |
100 mL 18.4 mol·L-1硫酸与足量铜反应,生成SO2的分子数为0.92NA |
C. |
1 L 0.1 mol·L-1的醋酸溶液中所含的离子和分子总数为0.1NA |
D. |
1.2 g NaHSO4晶体中阳离子和阴离子的总数为0.03NA |
|
下列说法正确的是 | |
| [ ] | |
A. |
自来水厂可用硫酸铁对水进行消毒杀菌 |
B. |
工业上通过电解AlCl3饱和溶液制备金属铝 |
C. |
蛋白质、葡萄糖和脂肪都可以在人体中发生水解 |
D. |
某温度下NH3(g)+HCl(g)=NH4Cl(s)能自发进行,则其ΔH<0 |
|
短周期元素A、B、C、D的原子序数依次递增,它们的原子序数之和为32,且原子最外层电子数之和为10;A、C原子的最外层电子数之和等于B原子的次外层电子数;A与C,B与D均为同主族元素.下列叙述正确的是 | |
| [ ] | |
A. |
四种元素的原子半径:A>B>C>D |
B. |
最高价氧化物对应的水化物的酸性:B>D |
C. |
C元素处于元素周期表中第3周期第ⅡA族 |
D. |
B、D的最高价氧化物中,B、D与氧原子之间均为单键 |
|
下列溶液中,离子一定能大量共存的是 | |
| [ ] | |
A. |
pH=l的溶液中:Na+、Mg2+、SO42-、HCO3- |
B. |
含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、SO42- |
C. |
加入Al能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
D. |
水电离产生的c(H+)=10-12 mol/L-1的溶液中:K+、Ba2+、NO3-、OH- |
|
设NA为阿伏加德罗常数的值,下列叙述正确的是 | |
| [ ] | |
A. |
0.1 mol/L的氯化铝溶液中含有的氯离子数为0.3NA |
B. |
常温下,1 mol O2和O3的混合气体中所含氧原子数为2.5NA |
C. |
标准状况下,11.2 L的乙烯中含有的共用电子对数为NA |
D. |
13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA |
|
下列有关物质性质的叙述正确的是 | |
| [ ] | |
A. |
浓硫酸能干燥氢气、氯气、一氧化碳等气体,说明浓硫酸具有吸水性 |
B. |
SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物 |
C. |
乙炔能使溴水、酸性高锰酸钾溶液褪色,说明乙炔具有漂白性 |
D. |
纤维素的水解产物能够发生银镜反应,说明纤维素是一种还原性糖 |
|
下列有关实验操作的叙述正确的是 | |
| [ ] | |
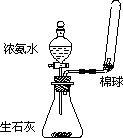
A. |
利用下图所示装置制取并收集氨气
|
B. |
用洁净的玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH |
C. |
用铂丝蘸取某溶液于无色火焰灼烧,火焰呈浅紫色,证明其中含K+ |
D. |
在苯和苯酚的混合液中加入足量的浓溴水,振荡、过滤分离出苯酚 |
|
在碘酸钠(NaIO3)的碱性溶液中通入氯气,可以得到高碘酸钠(Na2H3IO6).下列有关该反应的说法错误的是 | |
| [ ] | |
A. |
在该反应中碘酸钠作还原剂 |
B. |
碱性条件下,氯气的氧化性强于高碘酸钠 |
C. |
反应中生成1 mol Na2H3IO6,转移2 mol电子 |
D. |
反应中氧化产物与还原产物的物质的量之比为2∶1 |
|
下列实验方法不能达到目的的是 | |
| [ ] | |
A. |
用加热的方法分离氯化钠和氯化铵的固体混和物 |
B. |
用水鉴别乙醛、苯、硝基苯 |
C. |
用核磁共振氢谱鉴定未知物C2H6O的分子结构 |
D. |
用10 mL量筒量取5.00 mL 1.00 mol·L-1盐酸配制0.100 mol·L-1盐酸 |