|
下列反应的离子方程式书写正确的是 | |
| [ ] | |
A. |
铁屑溶于足量稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O |
B. |
碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-=CO32-+H2O |
C. |
金属钠溶于足量水中:Na+2H2O=Na++H2↑+2OH- |
D. |
苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
|
判断下列有关化学基本概念的依据正确的是 | |
| [ ] | |
A. |
溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
B. |
共价化合物:是否含有共价键 |
C. |
强弱电解质:溶液的导电能力大小 |
D. |
氧化还原反应:元素化合价是否变化 |
|
2008 年北京奥运会主体育场——“鸟巢”,被《泰晤士报》评为全球“最强悍”工程.“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓铟高亮度LED材料.有关说法正确的是
| |
| [ ] | |
A. |
合金的熔点通常比组分金属高,硬度比组分金属小 |
B. |
已知Ga处于ⅢA主族,可推知氮化镓化学式为Ga3N2 |
C. |
用金属铝与V2O5冶炼钒,铝作还原剂 |
D. |
ETFE膜( |
|
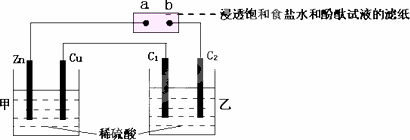
按下图所示装置进行实验(其中C1、C2均是石墨电极),下列说法中错误的是
| |
| [ ] | |
A. |
在标准状况下,Zn极减轻3.25 g时,Cu极上放出气体体积约为1.12 L |
B. |
发现a点附近显红色 |
C. |
在C1、C2电极所产生气体的体积比为2∶1 |
D. |
乙池溶液的pH减小 |
|
取pH均等于1的盐酸和醋酸各200 mL,分别稀释2倍,再分别加入0.6 g锌粉,在相同的条件下充分反应.有关叙述正确的是 | |
| [ ] | |
A. |
放出氢气一样多 |
B. |
醋酸与锌反应放出氢气多 |
C. |
反应速率一样快 |
D. |
盐酸与锌反应速率快 |
|
强氧化剂PbO2在酸性溶液中可将Mn2+氧化成MnO | |
| [ ] | |
A. |
充分振荡后静置,溶液颜色变为紫色 |
B. |
若上述实验完全反应,消耗PbO2的物质的量为0.01 mol |
C. |
上述实验不能用盐酸代替硫酸 |
D. |
在酸性条件下,PbO2的氧化性比MnO |
|
将等物质的量的X、Y气体充入一个密闭容器中,在一定条件下发生如下反应并达平衡:X(g)+Y(g) | |
| [ ] | |
A. |
升高温度,X的转化率增大 |
B. |
缩小容器体积,Z的浓度不变 |
C. |
保持压强不变,再充入0.1 mol X和0.1 mol Y,X的体积分数增大 |
D. |
保持容器体积不变,充入一定量的氦气,Y的浓度不变 |
|
下列实验基本操作正确的是 | |
| [ ] | |
A. |
滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定 |
B. |
将氢氧化钠固体放在纸片上称量 |
C. |
测定硫酸铜晶体结晶水含量时,加热后的坩埚须在干燥器中冷却,再称量 |
D. |
用玻璃棒蘸取溶液滴到湿润的pH试纸上,测其pH |