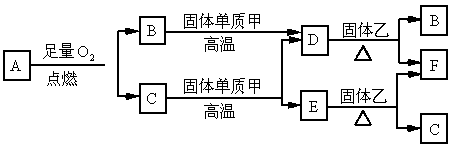
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家.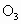 能吸收有害紫外线,保护人类赖以生存的空间.
能吸收有害紫外线,保护人类赖以生存的空间.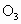 分子的结构如图所示,呈V形,键角为116.5°.三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子.请回答:
分子的结构如图所示,呈V形,键角为116.5°.三个原子以一个O原子为中心,与另外两个O原子分别构成一个共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键——三个O原子均等地享有这4个电子.请回答:
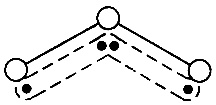
(1)臭氧与氧气的关系是________.
(2)下列分子与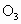 分子的结构最相似的是________.
分子的结构最相似的是________.
|
A. |
B. |
C. |
D. |
(3)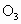 分子有________对孤对电子.
分子有________对孤对电子.
(4)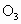 分子是否为极性分子________(填“是”或“否”).
分子是否为极性分子________(填“是”或“否”).
(5)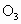 具有强氧化性,它能氧化PbS为
具有强氧化性,它能氧化PbS为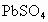 ,而
,而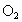 不能,试配平:
不能,试配平:
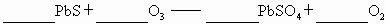
生成1mol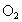 ,转移电子_______mol.
,转移电子_______mol.
(2005·上海)(A)
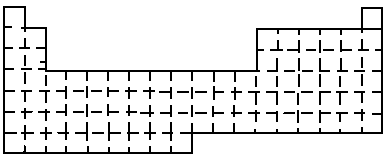
(1)在上面元素周期表中画出金属元素与非金属元素的分界线.
(2)根据NaOH的存在,有人提议可把氢元素放在ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的__________族.
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应呈黄色.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲元素与硫元素相比较,非金属性较强的是________(填名称),写出可以验证该结论的一个化学反应方程式_______.
(B)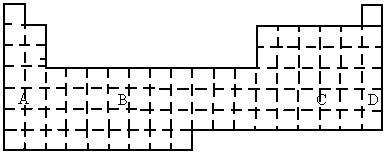
(1)在上面元素周期表中全部是金属元素的区域为_______.
|
a.A |
b.B |
c.C |
d.D |
(2)有人认为形成化合物最多的元素不是ⅣA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是______.
(3)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置.
②甲、乙两元素相比较,金属性较强的是__________(填名称),可以验证该结论的实验是___________.
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
 可以形成两种固体,一种为淡黄色,在水中的溶解度较小,另一种为黄绿色,在水中的溶解度较大.请回答下列问题:
可以形成两种固体,一种为淡黄色,在水中的溶解度较小,另一种为黄绿色,在水中的溶解度较大.请回答下列问题: 是平面正方形结构,还是四面体结构____________.
是平面正方形结构,还是四面体结构____________.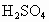 )分子的结构可表示为
)分子的结构可表示为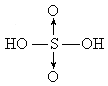 (其中“S→O”是特殊的共价键——配位键,共用的一对电子由S原子提供),而焦硫酸存在于发烟硫酸中,其分子式为
(其中“S→O”是特殊的共价键——配位键,共用的一对电子由S原子提供),而焦硫酸存在于发烟硫酸中,其分子式为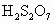 ,分子结构中不存在“—S—S—”键。请在注意了两者组成上的差别后,试写出焦硫酸分子的结构式________;在焦硫酸中,硫的化合价为________价.
,分子结构中不存在“—S—S—”键。请在注意了两者组成上的差别后,试写出焦硫酸分子的结构式________;在焦硫酸中,硫的化合价为________价.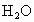
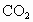
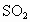
 为白色固体,溶于水显弱酸性,但它只是一元酸.可以用硼酸在水溶液中的电离平衡解释它只是一元酸的原因,请写出下面这个方程式右端的两种离子的表达式:
为白色固体,溶于水显弱酸性,但它只是一元酸.可以用硼酸在水溶液中的电离平衡解释它只是一元酸的原因,请写出下面这个方程式右端的两种离子的表达式: .
.