|
下列对熵的理解不正确的是 | |
| [ ] | |
A. |
同种物质气态时熵值最大,固态时熵值最小 |
B. |
体系越有序,熵值越小;越混乱,熵值越大 |
C. |
与外界隔离的体系,自发过程将导致体系的熵减小 |
D. |
25℃、1.01×105 Pa时,2N2O5(g) |
|
与实际化工生产流程相符的叙述是 | |
| [ ] | |
A. |
制备硝酸的工业中,理论上氨中的氮元素100%转化为了硝酸 |
B. |
制备硫酸的工业尾气用氢氧化钠溶液吸收 |
C. |
让Cl2在H2中燃烧制氯化氢,将氯化氢气体通入水中获得盐酸 |
D. |
工业上用电解熔融氯化铝和冰晶石的混合物的方法得到铝 |
|
下列说法正确的是 | |
| [ ] | |
A. |
根据K sp(AgCl)=1.77×10-10,Ksp(Ag2CrO4)=1.12×10-12,可以推知AgCl的溶解度比Ag2CrO4的溶解度大 |
B. |
0.1 mol·L-1的ZnCl2溶液中通入足量硫化氢气体,最终得不到ZnS沉淀.是因为溶液中c(Zn2+)·c(S2-)>K sp(ZnS) |
C. |
向硫酸钡沉淀中加入碳酸钠溶液,沉淀发生转化,据此可推知碳酸钡的K sp比硫酸钡的小 |
D. |
AgCl在10 mL 0.05 mol·L-1的KCl溶液中比在20 mL 0.01 mol·L-1的AgNO3溶液中溶解的质量少 |
|
已知Ca(OH)2的溶解度随温度升高而降低.将某温度下饱和澄清石灰水①加入少量生石灰后恢复到原来温度;②降低温度.这两种情况下,前后均保持不变的是 | |
| [ ] | |
A. |
溶液的质量 |
B. |
Ca(OH)2的溶解度 |
C. |
溶液中Ca2+离子的数目 |
D. |
溶液中溶质的质量分数 |
|
将AgCl分别加入盛有: ①5 mL水; ②6 mL 0.5 mol/L NaCl溶液; ③10 mL 0.2 mol/L CaCl2溶液; ④50 mL 0.1 mol/L盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是 | |
| [ ] | |
A. |
④③②① |
B. |
②③④① |
C. |
①④③② |
D. |
①③②④ |
|
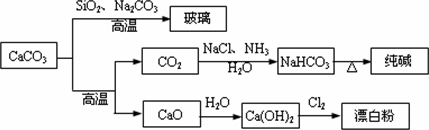
CaCO3是一种化工原料,可以通过反应生成一系列物质,如下图所示.
下列说法正确的是 | |
| [ ] | |
A. |
Cl2和SO2均可以漂白有色物质,且漂白的原理相同 |
B. |
由SiO2+Na2CO3 |
C. |
工业上,可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3 |
D. |
制取玻璃、纯碱和漂白粉所涉及的反应都是非氧化还原反应 |
|
将足量的AgI分别放入下列物质中,AgI的溶解度由大到小的排列顺序是 ①5 mL 0.001 mol·L-1 KI溶液 ②15 mL 0.002 mol·L-1 CaI2溶液 ③35 mL 0.003 mol·L-1 HI溶液 ④15mL蒸馏水 ⑤45 mL 0.005 mol·L-1 AgNO3溶液 | |
| [ ] | |
A. |
①>②>③>④>⑤ |
B. |
④>①>③>②>⑤ |
C. |
⑤>④>②>①>③ |
D. |
④>③>⑤>②>① |