|
1995年美国某教授报道,他制得了碳的第四种同素异形体——链式炔碳……C≡C≡C≡C≡C≡C……该物质一个分子中含300~500个碳原子,性质很活泼,据此判断,链式炔碳的熔点,估计比石墨 | |
| [ ] | |
A. |
低 |
B. |
相等 |
C. |
高 |
D. |
无法判断 |
|
氢化铵(NH4H)与氯化铵结构相似,又已知NH4H与水反应有氢气产生.下列叙述中不正确的是 | |
| [ ] | |
A. |
NH4H中有配位键 |
B. |
NH4H固体投入少量水中,有两种气体产生 |
C. |
NH4H中的H-半径比锂离子半径大 |
D. |
NH4H溶于水后,形成的溶液显酸性 |
|
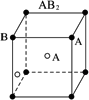
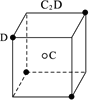
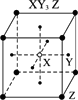
根据离子晶体的晶胞(晶体中最小的重复单位),求晶体中阴阳离子个数比的方法是: (1)处于顶点的离子,同时为8个晶胞共有,每个离子有1/8属于晶胞 (2)处于棱上的离子,同时为4个晶胞共有,每个离子有1/4属于晶胞 (3)处于面上的离子,同时为2个晶胞共有,每个离子有1/2属于晶胞 (4)处于内部的离子,则完全属于该晶胞 现有A、B、C、D四种晶体,离子的排列方式如下图所示,其中化学式不正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
电解NaCl-KCl-AlCl3熔体制铝比电解Al2O3-NaAlF6制铝节省电能约30%,但现在仍用后一种方法制铝,其主要原因是 | |
| [ ] | |
A. |
AlCl3是分子晶体,其熔体不导电 |
B. |
电解AlCl3生成的Cl2会严重污染大气 |
C. |
自然界不存在富含AlCl3的矿石 |
D. |
生产无水AlCl3较困难,成本又较高 |
|
1999年曾报道人们合成得到了含高能的正离子的化合物N5AsF6,下列叙述错误的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
化合物N5AsF6中砷元素化合价为+1价 |
D. |
化合物N5AsF6中氟元素化合价为-1价 |