|
某共价化合物含碳、氢、氮三种元素,已知其分子内的4个氮原子排列成内空的四面体结构,且每两个氮原子间都有一个碳原子,而无C-C单键、CC双键、C≡C三键,则它的分子式为 | |
| [ ] | |
A. |
C6H12N4 |
B. |
C4H8N4 |
C. |
C6H10N4 |
D. |
C6H8N4 |
|
实验测得BeCl2为共价化合物,两个Be-Cl键间的夹角为180°,由此可判断BeCl2属于 | |
| [ ] | |
A. |
由极性键形成的极性分子 |
B. |
由极性键形成的非极性分子 |
C. |
由非极性键形成的极性分子 |
D. |
由非极性键形成的非极性分子 |
|
N2F2存在顺式和反式两种异构体,据此事实,判断N2F2分子中两个氮原子之间的键型组成为 | |
| [ ] | |
A. |
仅有一个σ键 |
B. |
仅有一个π键 |
C. |
一个σ键,一个π键 |
D. |
两个π键 |
E. |
一个σ键,两个π键 |
|
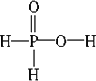
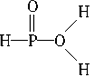
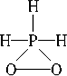
已知磷酸分子 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
已知HCN的空间构型为直线型,对于HCN分子中键的类型说法不正确的是 | |
| [ ] | |
A. |
分子内存在H-Cσ键是氢原子的s轨道与C的1个sp杂化轨道形成的 |
B. |
分子内存在着C-Nσ键 |
C. |
分子内CN之间除了有一个σ键外,还有两个π键 |
D. |
分子内只存在σ键 |
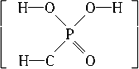 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可以跟D2O发生氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换.由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换.又知次磷酸(H3PO2)也可以跟D2O发生氢交换,但次磷酸钠(NaH2PO2)却不能再跟D2O发生氢交换.由此可推断出H3PO2的分子结构是