|
不久前,美国一个海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600-700℃,所用燃料为H2,电解质为熔融的K2CO3,已知该电池的总反应为2H2+O2 | |
A. |
正极反应为:4OH- |
B. |
放电时 |
C. |
电池供应1 mol水蒸气,转移电子数4 mol |
D. |
放电时 |
|
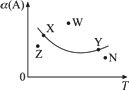
如图所示,是在其他条件一定时,反应2A+B
| |
A. |
X或Y两点相应v(正)=v(逆) |
B. |
Z、N两点表示未达平衡状态,且都是v(正)>v(逆) |
C. |
W点表示非平衡状态,v(正)>v(逆) |
D. |
相应反应速率大小的点:W>Y>N |
|
在一定温度下,将2 mol SO2和1 mol O2充入一定容积的密闭容器中,在催化剂作用下发生如下反应:2SO2(g)+O2(g) | |
A. |
生成SO3 2 mol |
B. |
放出197 kJ热量 |
C. |
SO2和SO3共2 mol |
D. |
含氧元素8 mol |
|
已知常温常压下,N2(g)和H2(g)生成2 mol NH3(g)放出92.4 kJ热量.在同温同压下向密闭容器中通入1 mol N2和3 mol H2,达到平衡时放出热量为Q1 kJ,向另一体积相同的密闭容器中通入0.5 mol N2、1.5 mol H2和1 mol NH3,相同条件下达到平衡时放出热量为Q2 kJ,则下列关系式正确的是 | |
A. |
2Q2=Q1=92.4 |
B. |
Q2<Q1<92.4 |
C. |
Q1<Q2<92.4 |
D. |
Q1=Q2<92.4 |
|
X、Y是元素周期表ⅦA族中的两种元素.下列叙述能说明X的非金属性比Y强的是 | |
A. |
X原子的电子层数比Y原子的电子层数多 |
B. |
X的氢化物的沸点比Y的氢化物的沸点低 |
C. |
X的气态氢化物比Y的气态氢化物稳定 |
D. |
Y的单质能将X从NaX的溶液中置换出来 |