|
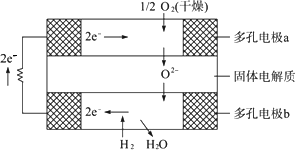
固体氧化物燃料电池是由美国西屋(Westing-house)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是
| |
A. |
有O2放电的a极为电池的负极 |
B. |
有H2放电的b极为电池的正极 |
C. |
a极对应的电极反应为O2+2H2O+4e- |
D. |
该电池的总反应方程式为2H2+O2 |
|
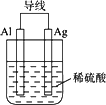
我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为:4Al+3O2+6H2 | |
A. |
正极反应式为:O2+2H2O+4e- |
B. |
电池工作时,电流由铝电极沿导线流向铂电极 |
C. |
以网状的铂为正极,可增大与氧气的接触面积 |
D. |
该电池通常只需更换铝板就可继续使用 |
|
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池说法正确的是 | |
A. |
在熔融电解质中,O2-由负极移向正极 |
B. |
电池的总反应是2C4H10+13O2 |
C. |
通入空气的一极是正极,电极反应为:O2+4e- |
D. |
通入丁烷的一极是正极,电极反应为:C4H10+26e-+13O2- |
|
银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可表示为2Ag+Zn(OH)2 在此电池放电时,负极上发生反应的物质是 | |
A. |
Ag |
B. |
Zn(OH)2 |
C. |
Ag2O |
D. |
Zn |
|
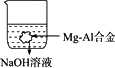
关于下图,以下说法正确的是
| |
A. |
上图构成原电池,Mg为负极 |
B. |
电池的总反应为:2Al+2NaOH+2H2O |
C. |
当转移0.004 mol电子时产生0.001 mol O2 |
D. |
反应结束后pH降低 |
|
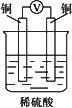
根据下列事实: (1)X+Y2+ (2)Z+2H2O(冷) (3)Z2+比X2+氧化性弱 (4)由Y、W电极组成的原电池电极反应:W2++2e- 可知:X、Y、Z、W还原性由强到弱的顺序是 | |
A. |
X>Z>Y>W |
B. |
Z>W>X>Y |
C. |
Z>X>Y>W |
D. |
Z>Y>X>W |
|
电子表所用纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应如下:锌极:Zn+2OH--2e- | |
A. |
锌为正极,被氧化 |
B. |
Ag2O是正极,发生还原反应 |
C. |
电子从负极流向Ag2O极 |
D. |
Zn为负极,被还原 |